Xơ phổi
Trong bài viết này, chúng tôi sẽ thảo luận về các bệnh lý phổi có dạng lưới và cung cấp hướng dẫn cho các bác sĩ X quang trong việc đánh giá các bệnh phổ biến nhất cùng các dạng tổn thương của chúng.
Một phương pháp tiếp cận từng bước được trình bày nhằm xác định các đặc điểm chính trong bệnh phổi xơ hóa và giúp đưa ra chẩn đoán phân biệt dễ dàng hơn.
Chúng tôi xin cảm ơn Nestor L. Müller vì những nhận xét của ông về bản thảo.
Lung anatomy
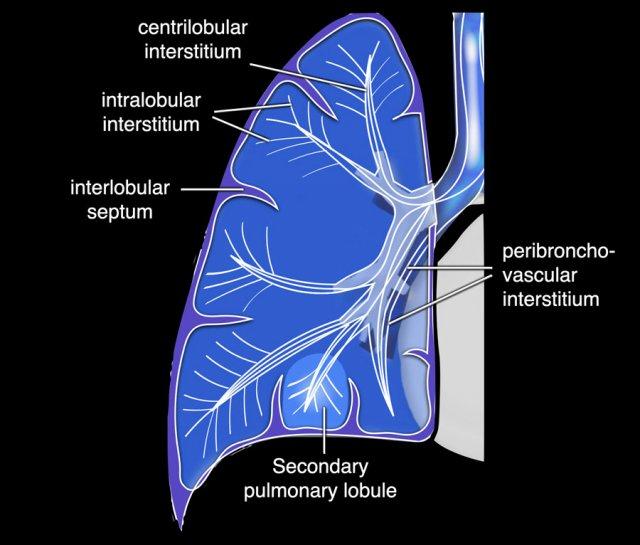
Giải phẫu của bệnh phổi dạng lưới liên quan đến mô kẽ phổi, là một cấu trúc liên tục bao gồm cả thành phần ngoại vi và thành phần trục (hình).
Mô kẽ ngoại vi nâng đỡ các tiểu thùy thứ cấp xa và bao gồm các vùng dưới màng phổi và quanh khe liên thùy, trong khi mô kẽ trục nâng đỡ các cấu trúc phế quản-mạch máu từ rốn phổi hướng ra ngoại vi.
Mô kẽ cũng chứa các mạch bạch huyết của phổi. Trong điều kiện bình thường, bản thân mô kẽ nằm dưới ngưỡng phân giải của CT.
Sự dày lên của mô kẽ là cơ chế nền tảng tạo nên hình ảnh dạng lưới.
Bảng thuật ngữ Fleischner [1] định nghĩa hình lưới là “tập hợp vô số các đám mờ dạng đường nhỏ mà khi chồng lên nhau tạo ra hình ảnh giống như một tấm lưới”.
Stepwise Approach
Bước
đầu tiên là xác định liệu hình ảnh lưới có thực sự đại diện cho xơ hóa hay không.
Bước
tiếp theo là xác định xem đó là kiểu UIP chắc chắn, có thể hoặc không xác định,
hay một kiểu thay thế khác.
Nếu
đó là UIP chắc chắn hoặc có thể, cần nhận thức rằng không phải tất cả UIP đều
bằng xơ phổi vô căn, vì UIP có/không có tổ ong cũng có thể gặp trong
sarcoid xơ hóa, viêm phổi quá mẫn, và bệnh phổi kẽ liên quan đến bệnh mô liên kết
giai đoạn cuối (CTD-ILD).
Step 1 – Is it really fibrosis?
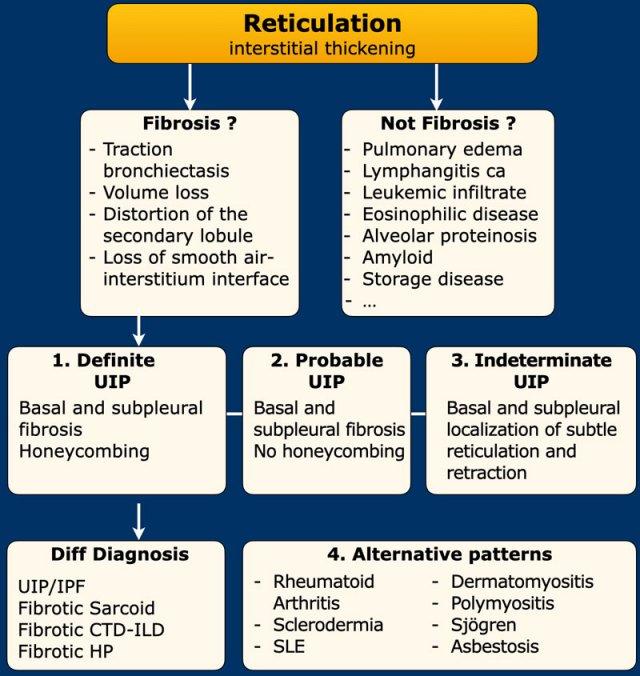
Xơ hóa gây co kéo các cấu trúc xung quanh và sẽ dẫn đến:
- Volume loss
- Bronchiectasis
- Distortion of the secondary lobule
- Loss of the smooth air-to-interstitium interfaces
Do đó, đây là những đặc điểm đầu tiên cần tìm kiếm khi đánh giá liệu hình ảnh lưới có đại diện cho xơ hóa phổi hay không.
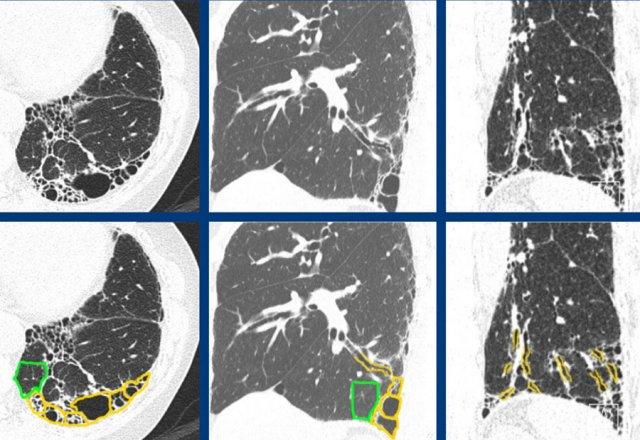
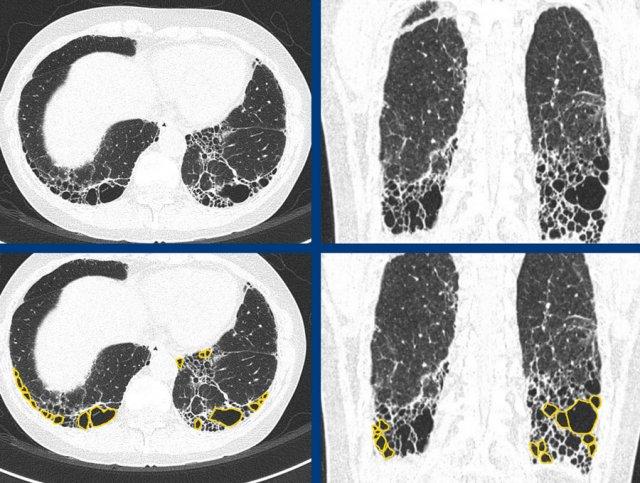
Hình ảnh cho thấy bệnh phổi xơ hóa với sự biến dạng của tiểu thùy thứ cấp, mất thể tích và giãn phế quản do co kéo (màu xanh lá là bình thường, màu vàng là bất thường).
Không phải tất cả các dạng lưới đều là xơ hóa, vì mô kẽ phổi có thể bị dày lên do các bệnh lý khác.
Most
commonly this is:
- Dịch do phù phổi.
Nhưng
cũng có thể gặp trong ví dụ như: - Tế bào ác tính trong ung thư biểu mô dạng bạch mạch, hoặc thâm nhiễm bạch cầu
- Protein trong bệnh protein phế nang, amyloid và bệnh tích lũy
- Benign cells in eosinophilic
lung disease
Các
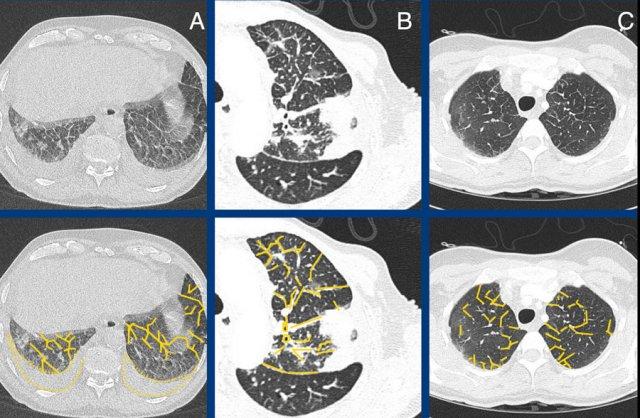
hình ảnh minh họa các ví dụ về lưới không xơ hóa do dày thành kẽ trong phù phổi (A), ung thư biểu mô di căn đường bạch huyết (B), và浸润 bạch cầu ái toan trong u hạt bạch cầu ái toan kèm viêm đa mạch [EGPA,
trước đây gọi là hội chứng Churg-Strauss] (C).
ILA -interstitial lung abnormalities
Những thay đổi mô kẽ nhẹ tình cờ phát hiện – ở những bệnh nhân không có biểu hiện lâm sàng nghi ngờ bệnh phổi kẽ (ILD) – được gọi là ‘bất thường phổi kẽ (ILA)’.
Những thay đổi không xác định và nhỏ này có thể đại diện cho giai đoạn sớm của bệnh phổi kẽ xơ hóa, nhưng cũng có thể chỉ là một số sẹo sau nhiễm trùng hoặc những thay đổi kẽ nhẹ liên quan đến hút thuốc hoặc tuổi tác.
Ngưỡng cắt 5% tổn thương phổi đã được đề xuất như một tiêu chí phân biệt bệnh lý có ý nghĩa lâm sàng [2], tuy nhiên, việc đánh giá trực quan chính xác là rất khó khăn.
Theo dõi có thể cho thấy đây có phải là phát hiện tình cờ có liên quan hay không, điều này là tùy chọn và phụ thuộc vào đặc điểm của bệnh nhân.
Step 2 – UIP pattern
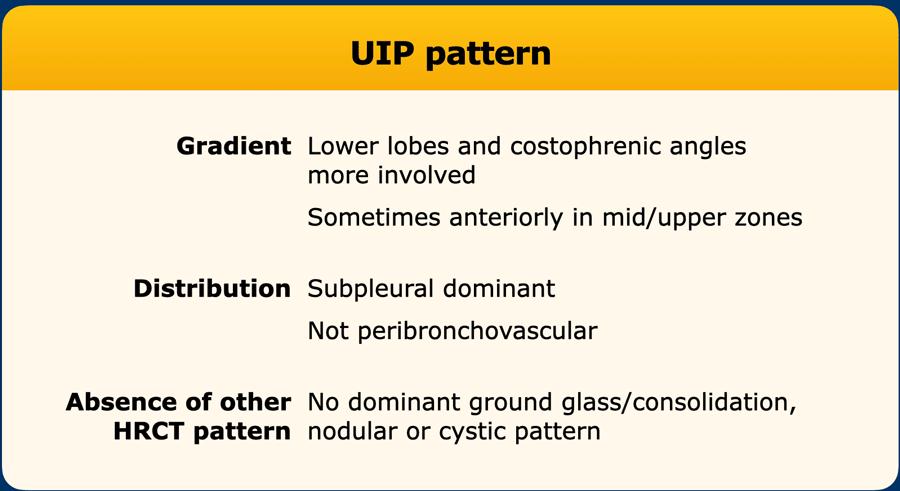
Kiểu hình UIP dựa trên gradient tổn thương, phân bố của xơ hóa và sự vắng mặt của kiểu hình HRCT chiếm ưu thế khác.
Các
dạng tổn thương trên HRCT khác như kính mờ, nang phổi, nốt centrilobular hoặc
nốt quanh bạch mạch và đông đặc phổi cần vắng mặt, vì những dạng này liên quan
đến các bệnh lý nền khác và không ủng hộ chẩn đoán UIP/IPF.
Đầu tiên, xơ hóa phải có gradient hướng về phía đáy phổi, với thùy dưới và góc sườn hoành bị tổn thương nhiều hơn so với vùng phổi giữa và trên.
Xơ hóa có thể nằm hơi về phía trước hơn ở vùng phổi giữa/trên, được gọi là ‘dấu hiệu cánh quạt’, theo hình xoắn hiện diện trong cánh của một chiếc chân vịt.
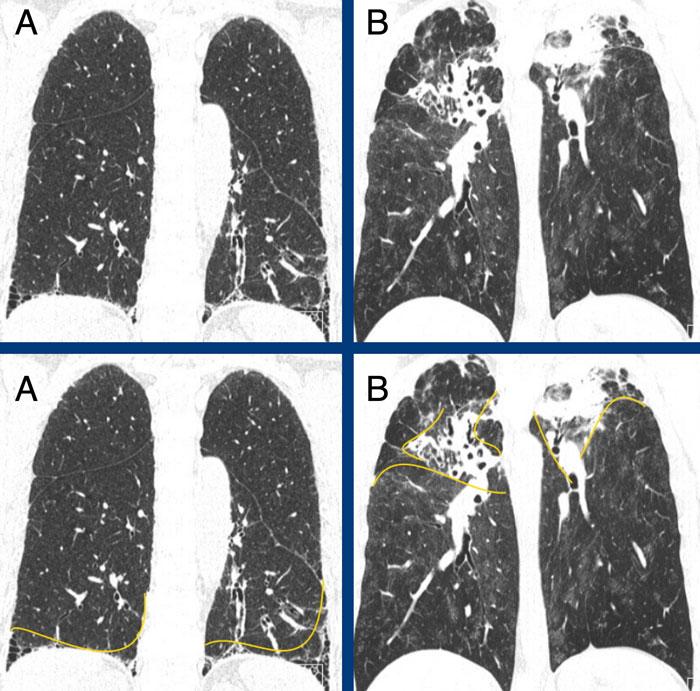
Các hình ảnh cho thấy tổn thương xơ hóa ưu thế ở vùng đáy phổi và dưới màng phổi trong A, so với tổn thương xơ hóa ưu thế ở vùng đỉnh phổi và trung tâm trong B.
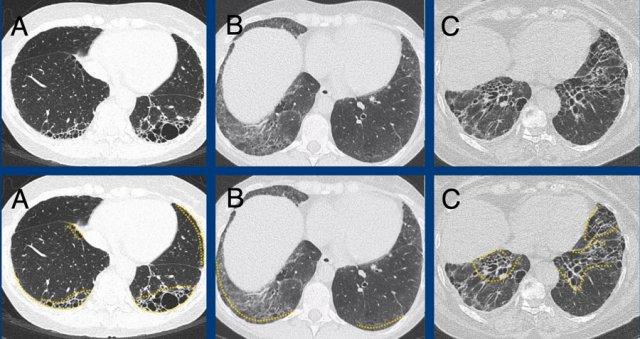
Subpleural dominant (A), subpleural sparing (B), and peribronchial dominant (C) patterns of fibrosis.
Thứ hai, xơ hóa phải có dạng chiếm ưu thế dưới màng phổi. Điều này có nghĩa là bệnh nhắm vào mô kẽ ngoại vi và tổn thương phổi ngay bên dưới màng phổi.
Bệnh không được bỏ qua mô phổi dưới màng phổi, cũng không được tập trung xung quanh bó phế quản-mạch máu (tức là không được tổn thương chủ yếu ở mô kẽ trục).
UIP classification
Có các hướng dẫn chẩn đoán hình ảnh cụ thể để đánh giá UIP/IPF – được ban hành bởi sự hợp tác của các Hội Lồng ngực trên toàn thế giới (ATS/ERS/JRS/ALAT) cũng như bởi Hội Fleischner [3,4].
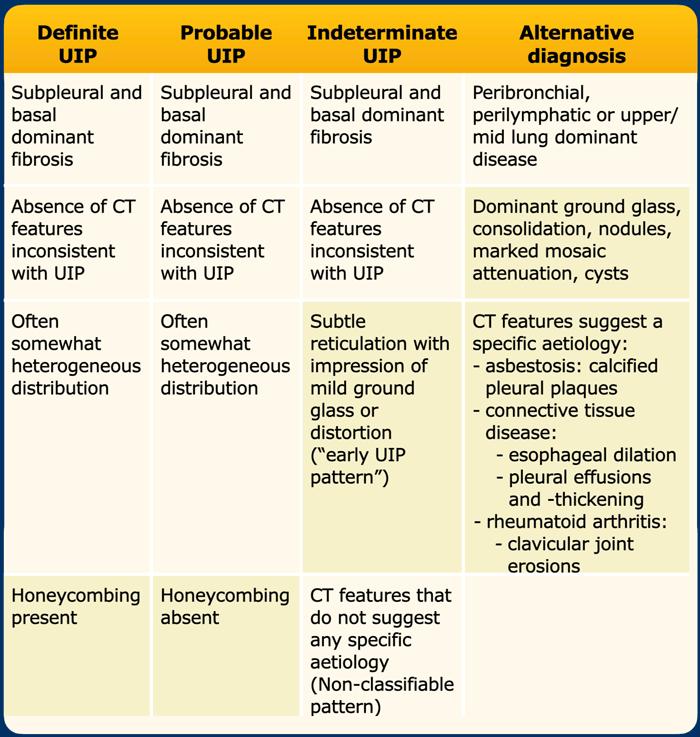
Điểm mấu chốt của cả hai hướng dẫn là chẩn đoán hình ảnh HRCT cần đưa ra kết luận về một trong các trường hợp sau:
- Definite UIP pattern
- Probable UIP pattern
- Indeterminate UIP pattern
- Suggestive of another diagnosis than UIP/IPF
Ở bệnh nhân có xơ hóa ưu thế vùng đáy và dưới màng phổi, không có các đặc điểm phụ trợ không phù hợp, sự hiện diện hay vắng mặt của tổ ong sẽ quyết định việc phân loại là dạng UIP xác định hay có thể.
Tuy nhiên, việc đánh giá tổ ong có thể gặp phải sự biến thiên đáng kể giữa các quan sát viên, ngay cả giữa các chuyên gia [5].
Tổ ong trên hình ảnh CT được định nghĩa là “các khoang khí dạng nang tập hợp theo hướng dưới màng phổi, thường có kích thước khoảng 3-10 mm”.
Cần lưu ý rằng đây là khác biệt so với tổ ong quan sát thấy trên mô bệnh học, được định nghĩa là “mô phổi bị phá hủy và xơ hóa chứa nhiều khoang khí dạng nang với thành xơ dày, kèm mất hoàn toàn cấu trúc tiểu thùy” [1].
Mặc dù cả hai đều đại diện cho tình trạng xơ hóa đã hình thành và nặng nề, chúng được quan sát ở các mức độ phóng đại khác nhau đáng kể.
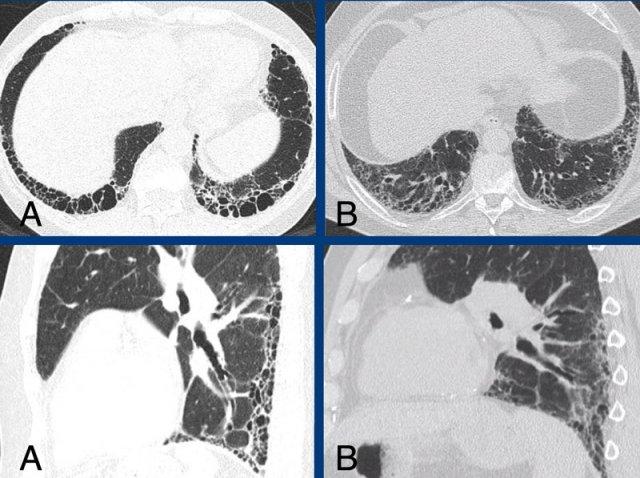
Trong A có hình ảnh tổ ong kết hợp với xơ hóa ưu thế ở nền phổi và dưới màng phổi, cho thấy hình thái UIP điển hình.
In B there is a probable UIP pattern without honeycombing.
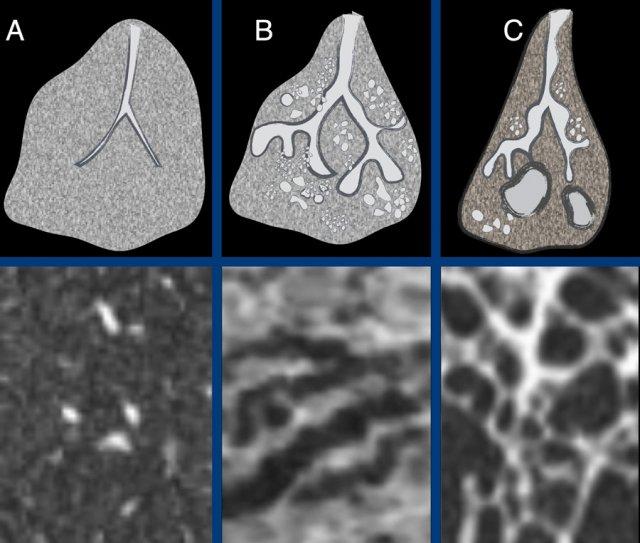
The ongoing process of honeycombing formation. There is a spectrum ranging from normal lung tissue (A), through distortion of the secondary lobule with traction bronchiolectasis (B), to end stage cyst formation (C).
Tổ ong
là kết quả của xơ hóa tiến triển kèm theo biến dạng cấu trúc và nằm ở cuối thang điểm từ mô phổi bình thường, qua biến dạng tiểu thùy thứ cấp với giãn phế quản nhỏ do co kéo, đến hình thành nang giai đoạn cuối.
Mặc dù
sự hiện diện của tổ ong xác định sự khác biệt giữa thể UIP có thể và thể UIP chắc chắn,
tổ ong không phải là dấu hiệu đặc trưng của bệnh xơ phổi vô căn
(IPF) vì nó chỉ là một đặc điểm của xơ hóa nặng.
Tổ ong
cũng có thể xuất hiện trong giai đoạn xơ hóa (giai đoạn cuối) của bệnh sarcoidosis, NSIP và
viêm phổi quá mẫn. Tóm lại, hình ảnh UIP không đồng nghĩa với IPF.
Tuy nhiên,
trong bối cảnh lâm sàng phù hợp ở bệnh nhân được nghi ngờ lâm sàng mắc xơ phổi vô căn (IPF), hình ảnh UIP điển hình sẽ xác định chẩn đoán (tức là chẩn đoán UIP/IPF), loại bỏ nhu cầu thực hiện các xét nghiệm xâm lấn thêm như sinh thiết phổi qua nội soi phế quản bằng đầu dò lạnh hoặc sinh thiết phổi phẫu thuật.
Step 3 – Alternative Patterns
– Axial and non-basal distribution
Axial and non-basal distribution
Khi
bệnh lý mô kẽ không chủ yếu ở dưới màng phổi mà phân bố chủ yếu quanh phế quản,
hai chẩn đoán cần cân nhắc hàng đầu là viêm phổi quá mẫn (HP) mạn tính thể xơ hóa
và bệnh sarcoidosis.
Ưu thế thùy đỉnh thường gặp trong bệnh sarcoidosis, nhưng chỉ gặp ở một số ít trường hợp viêm phổi quá mẫn mạn tính.
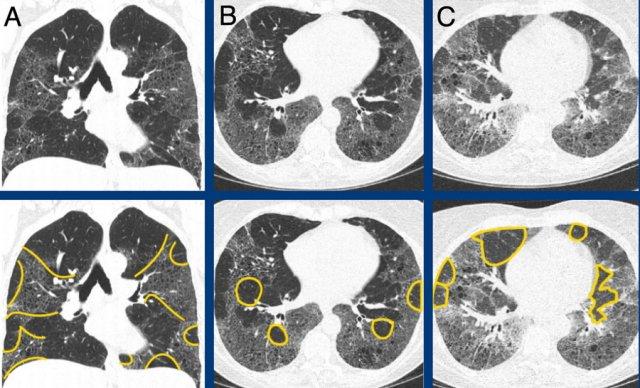
Typical fibrotic hypersensitivity pneumonitis showing diffuse non-basal dominant (A), peribronchial orientated ground-glass and mild fibrotic changes with mosaicism (A and B), and expiratory air trapping (C).
Hypersensitivity pneumonitis
HP mạn tính xơ hóa điển hình được đặc trưng bởi xơ hóa quanh phế quản với các mức độ kính mờ khác nhau và suy giảm khảm rõ rệt do sự bảo tồn của các tiểu thùy thứ cấp.
Bẫy khí thì thở ra do tắc nghẽn đường thở nhỏ là một dấu hiệu đặc trưng.
Các nốt kính mờ trung tiểu thùy có thể xuất hiện, nhưng thường gặp hơn và chiếm ưu thế ở giai đoạn bán cấp (không xơ hóa) của bệnh.
Xơ
hóa có thể có phân bố ngẫu nhiên hoặc lan tỏa, hoặc ưu thế ở vùng phổi giữa hoặc trên với tương đối ít tổn thương ở vùng đáy phổi.
Sarcoidosis
Sarcoidosis
is the great mimicker.
Xơ hóa trong bệnh sarcoidosis thường có biểu hiện ưu thế ở vùng quanh phế quản mạch máu và vùng phổi giữa đến trên với biến dạng cấu trúc và giãn phế quản do co kéo trung tâm, kèm theo một lượng thay đổi của dạng lưới và đôi khi thậm chí có tổ ong.
Mặc dù
sarcoidosis ban đầu thường biểu hiện với hạch bạch huyết rốn phổi hai bên và trung thất, nhưng ở giai đoạn xơ hóa muộn của bệnh, các hạch thường có kích thước bình thường và bị vôi hóa.
Các
hình ảnh cho thấy bệnh sarcoidosis xơ hóa điển hình với tổn thương ưu thế quanh phế quản-mạch máu và vùng đỉnh, biểu hiện dạng nốt (hợp lưu), lưới và kính mờ nhẹ, cùng với giãn phế quản do co kéo lan rộng.
– Ground-glass pattern and Consolidation
Ground-glass
Mặc dù có thể thấy một số kính mờ ở các vùng có dạng lưới – một dấu hiệu không loại trừ chẩn đoán kiểu UIP có thể – nhưng thành phần kính mờ chiếm ưu thế gợi ý một chẩn đoán thay thế khác.
Kính mờ có thể gợi ý một loạt các bệnh lý, bao gồm bệnh mô liên kết (CTD) liên quan đến ILD, viêm phổi quá mẫn, cũng như ILD liên quan đến hút thuốc và thuốc.
Kính mờ thường là đặc điểm của thể viêm phổi kẽ không đặc hiệu (NSIP).
Kính mờ thuần túy không có thay đổi xơ hóa là đặc điểm nổi bật của NSIP thể tế bào, được phân biệt với thể NSIP xơ hóa trong đó có lưới, giãn phế quản do co kéo và biến dạng cấu trúc do xơ hóa.
NSIP thường chiếm ưu thế ở vùng đáy phổi với hình ảnh kính mờ rõ rệt, lưới và giãn phế quản nhỏ do co kéo. Bảo tồn dưới màng phổi ở vùng lưng của thùy dưới chỉ xuất hiện trong khoảng 40% trường hợp và có thể là một đặc điểm hữu ích trong việc chẩn đoán.
Consolidations
Các vùng đông đặc không phải là một phần của hình ảnh UIP có thể. Các vùng xơ hóa nhỏ khu trú có thể gặp trong UIP, tuy nhiên, vùng đông đặc đáng kể hơn trên hình ảnh HRCT thường do thành phần viêm phổi tổ chức hóa và gợi ý chẩn đoán khác ngoài UIP/IPF.
Nhiễm trùng phổi tiến triển hoặc ác tính luôn cần được xem xét.
Connective tissue disease related ILD
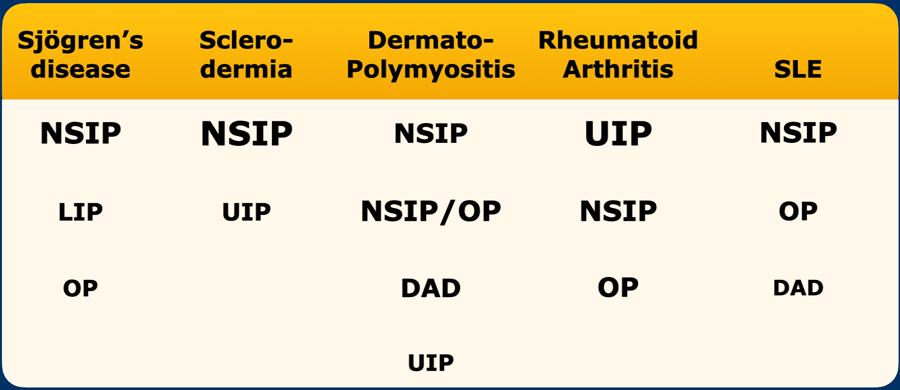
Bảng hiển thị các dạng hình ảnh trong bệnh phổi kẽ liên quan đến bệnh mô liên kết (CTD-ILD), trong đó kích thước phông chữ tương quan với tần suất của từng dạng hình ảnh.
Bệnh phổi kẽ liên quan đến bệnh mô liên kết (CTD-ILD) có thể biểu hiện với nhiều dạng tổn thương khác nhau.
Trong nhóm bệnh không đồng nhất này, các biểu hiện bệnh với dạng tổn thương NSIP cùng với các thành phần khác như đông đặc dạng vòm cung do viêm phổi tổ chức hóa (OP) hoặc nang do viêm phổi kẽ lympho bào (LIP) có thể gợi ý một chẩn đoán cụ thể (xem Bảng).
NSIP
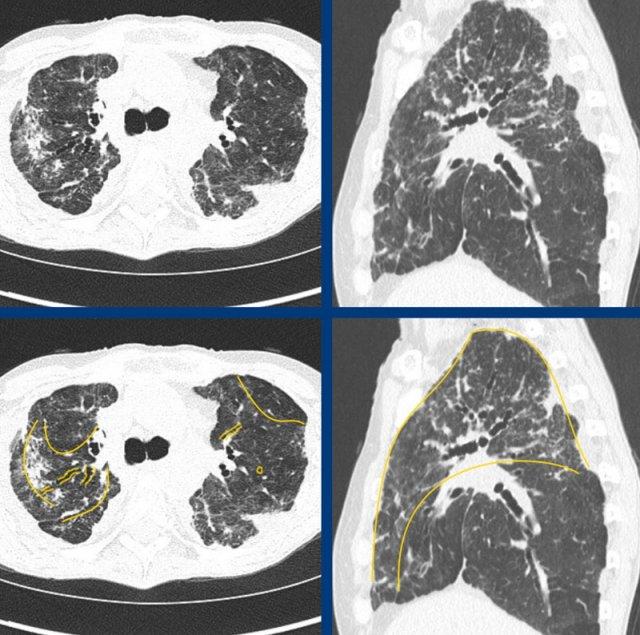
Hình ảnh NSIP xơ hóa điển hình trong bệnh Sjögren với các thay đổi xơ hóa và kính mờ chiếm ưu thế theo phân bố đáy phổi, lan rộng ra phần trung tâm.
Subpleural
sparing is not a dominant feature in this case.
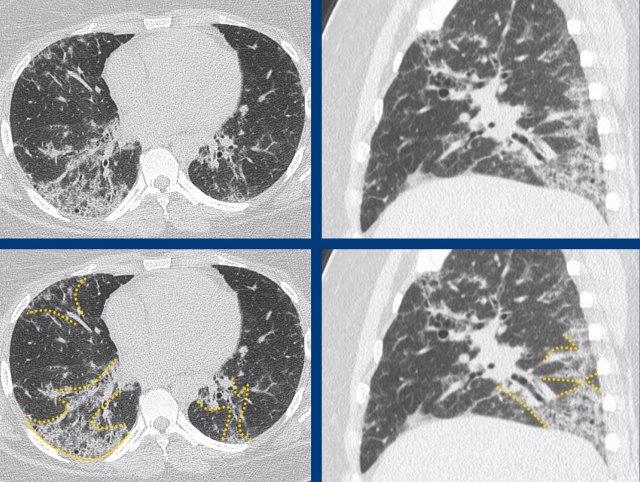
Các hình ảnh cho thấy sự kết hợp giữa kính mờ ưu thế nền phổi và giãn phế quản do co kéo, kết hợp với các vùng đông đặc dạng cung quanh tiểu thùy giới hạn do viêm phổi tổ chức hóa (OP) đồng thời.
Chẩn đoán cuối cùng là NSIP xơ hóa trong hội chứng kháng synthetase.
Hội chứng kháng synthetase là một rối loạn đa hệ thống qua trung gian miễn dịch có thể bao gồm (trong số các biểu hiện khác) bệnh phổi kẽ, viêm cơ và/hoặc viêm đa khớp, thay đổi da và hiện tượng Raynaud.
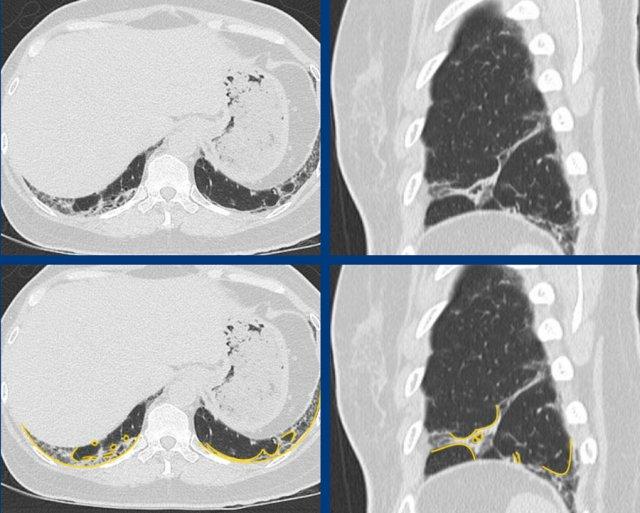
Rheumatoid Arthritis
Những thay đổi xơ hóa nặng theo hướng ưu thế dưới màng phổi và đáy phổi, với hình ảnh tổ ong lan rộng, phù hợp với mô hình UIP do viêm khớp dạng thấp (RA).
Viêm khớp dạng thấp có thể biểu hiện tổn thương đa khoang và dẫn đến bệnh lý đường thở, bệnh lý màng phổi và bệnh phổi kẽ, thường gặp nhất với dạng UIP (viêm phổi kẽ thông thường).
Smoking-related ILD
Bệnh phổi kẽ liên quan đến hút thuốc là một phân nhóm khó, thường biểu hiện khí phế thũng nặng với những thay đổi xơ hóa chồng lấp nhẹ hơn, các bất thường lan tỏa hơn hoặc ưu thế ở vùng đỉnh, mất thể tích vùng đáy ít nghiêm trọng hơn và nhiều kính mờ hơn so với thể UIP (có thể) điển hình.
Tuy nhiên, những thay đổi ở phổi liên quan đến hút thuốc thường đồng thời xuất hiện với các bệnh phổi kẽ khác, do một số lượng đáng kể bệnh nhân mắc bệnh phổi kẽ là những người đang hoặc đã từng hút thuốc lá.
Người hút thuốc hiếm khi mắc HP mạn tính, trong khi đây là yếu tố nguy cơ cá nhân đối với UIP/IPF.
Xơ hóa mô kẽ liên quan đến hút thuốc (SRIF) và xơ hóa phổi kết hợp khí phế thũng (CPFE) là các thuật ngữ thường được sử dụng, tuy nhiên, chúng chưa được định nghĩa chặt chẽ như các dạng tổn thương trên X-quang.
Drug-induced ILD
Bệnh phổi kẽ do thuốc là một phân nhóm khó chẩn đoán với các đặc điểm hình ảnh thường không đặc hiệu.
Cần luôn xem xét trong mọi chẩn đoán phân biệt, đặc biệt trong các trường hợp có dạng không phải UIP.
Theo kinh điển, bệnh phổi kẽ do thuốc thường liên quan đến dạng kính mờ chiếm ưu thế và/hoặc dạng đông đặc viêm phổi tổ chức, nhiều hơn là xơ hóa thực sự.
Methotrexate, Amiodarone và Nitrofurantoin là những ví dụ điển hình về các thuốc gây độc phổi, mặc dù danh sách này còn được ghi nhận thêm rất nhiều loại khác.
So với các thập kỷ trước, việc sử dụng ngày càng nhiều liệu pháp miễn dịch có thể khiến chúng ta gặp các dạng viêm phổi do thuốc thường xuyên hơn.
Xem www.pneumotox.com để biết thêm thông tin về các thuốc gây độc phổi và các dạng hình ảnh học liên quan đã được báo cáo.
Radiologically non-classifiable disease
Không hiếm gặp trường hợp các phát hiện trên HRCT không phù hợp với một trong những dạng hình ảnh X quang đã được biết đến.
Điều này có thể do những thay đổi mô kẽ hạn chế và không đặc hiệu, hoặc do sự kết hợp của các đặc điểm thực sự không xác định được.
Ví dụ, có thể có dạng lưới ưu thế dưới màng phổi và giãn phế quản do co kéo, nhưng không có gradient rõ ràng hoặc thành phần kính mờ không rõ ràng và không có các phát hiện bổ sung nào khác để gợi ý một chẩn đoán cụ thể.
Thường có quan niệm rằng việc không đưa ra kết luận về một dạng hình ảnh cụ thể là biểu hiện của sự thiếu quyết đoán, tuy nhiên cần nhấn mạnh rằng “bệnh không phân loại được trên X quang” cũng là một kết luận hoàn toàn hợp lệ trong báo cáo HRCT.
Trên thực tế, kết luận này còn tốt hơn nhiều so với “có thể là UIP, chẩn đoán phân biệt NSIP hoặc HP”.
Multidisciplinary approach
Chẩn đoán một bệnh điển hình dựa trên các hình ảnh học đặc trưng không phải là điều thường gặp.
Thay vào đó, việc đưa ra chẩn đoán phân biệt phổ biến hơn vì các đặc điểm hình ảnh học có thể không đặc hiệu.
Trong một nhóm đa chuyên khoa, các hình ảnh học có thể được đối chiếu với thông tin lâm sàng, kết quả đo chức năng hô hấp, kết quả xét nghiệm, kết quả rửa phế quản phế nang và sinh thiết phổi để đạt được chẩn đoán đồng thuận và kế hoạch điều trị.
Clinical information
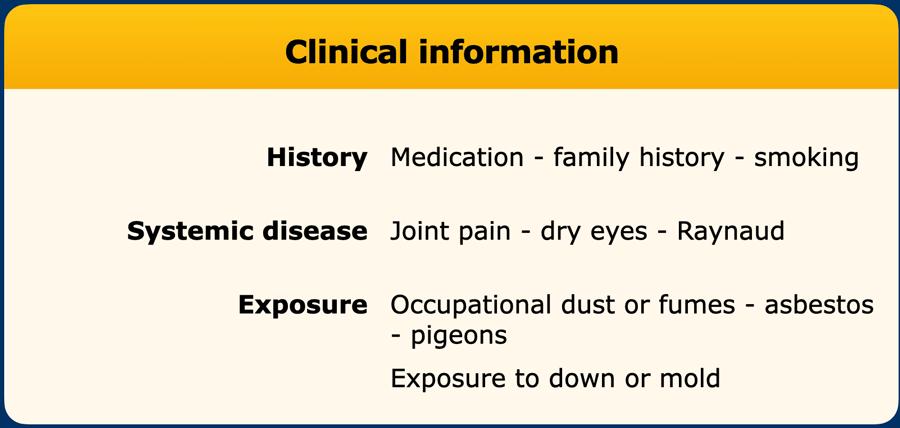
Trong
quá trình đánh giá bệnh nhân ILD, thông tin lâm sàng được thu thập (bảng)
Mặc dù
có hơn 200 tác nhân được ghi nhận có liên quan đến viêm phổi quá mẫn mạn tính,
nhưng kết quả phân tích phơi nhiễm nghề nghiệp và môi trường thường còn hạn chế.
Pulmonary Function Tests
Hiểu biết cơ bản về cơ chế của các bài kiểm tra chức năng phổi là rất hữu ích.
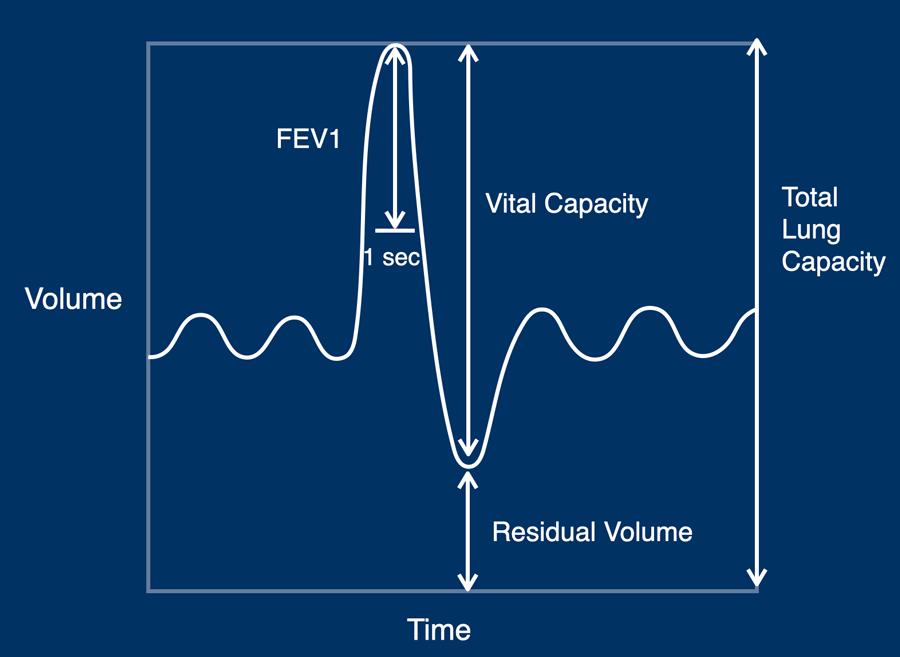
Có ba thành phần chính trong kiểm tra chức năng phổi:
- Static lung volumes (TLC, RV, VC)
- Spirometry (forced expiratory flow in 1 second’ (FEV1)
- Diffusion capacity for carbon monoxide (DLCO)
Index parameters in static lung volume assessment are:
- TLC: dung tích toàn phổi, là tổng thể tích của phổi sau khi hít vào tối đa
- RV: thể tích khí cặn, là thể tích phổi ở cuối thì thở ra tối đa
- VC: dung tích sống, là hiệu số giữa TLC và RV
Thông thường, thể tích phổi giảm trong bệnh phổi hạn chế (ví dụ: xơ phổi, bệnh thần kinh cơ) và tăng trong bệnh phổi tắc nghẽn (ví dụ: COPD, hen suyễn).
DLCO đo khả năng trao đổi khí carbon monoxide, và là chỉ số thay thế phản ánh khả năng oxy được vận chuyển vào máu.
DLCO tỷ lệ thuận với diện tích bề mặt màng phế nang-mao mạch và tỷ lệ nghịch với độ dày của màng phế nang-mao mạch.
Thông thường, DLCO giảm trong các bệnh lý làm giảm diện tích bề mặt màng (ví dụ: khí phế thũng, bệnh huyết khối tắc mạch) hoặc làm dày màng khuếch tán (ví dụ: xơ phổi).
Kiểu mẫu PFT điển hình trong xơ hóa phổi là hạn chế, cho thấy kết quả đo phế dung tương đối bình thường với thể tích phổi và DLCO giảm.
Tuy nhiên, có thể gặp kiểu mẫu hỗn hợp ở những bệnh nhân có cả hai thành phần bệnh hạn chế và tắc nghẽn.
Ví dụ, các giai đoạn tiến triển của viêm phổi quá mẫn mạn tính hoặc sarcoidosis có thể biểu hiện đồng thời cả bệnh đường thở nhỏ lẫn xơ hóa phổi.
Ngoài ra, sự đóng góp cộng gộp của khí phế thũng và xơ hóa trong ‘xơ hóa phổi kết hợp khí phế thũng’ (CPFE) có thể dẫn đến hiện tượng ‘bình thường hóa giả’ của kết quả đo phế dung và thể tích phổi, trong khi các triệu chứng lâm sàng và DLCO thường bất thường một cách rõ rệt.
Laboratory analysis
Việc tìm kiếm các dấu ấn viêm và tự kháng thể là một phần trong đánh giá tiêu chuẩn của ILD.
Điều quan trọng cần nhận thức là sự hiện diện của một tự kháng thể không đồng nghĩa với chẩn đoán bệnh tự miễn.
Thay vào đó, huyết thanh học dương tính giúp hỗ trợ chẩn đoán nếu đi kèm với các dấu hiệu và triệu chứng lâm sàng phù hợp.
Common biomarkers are:
- Yếu tố dạng thấp (RF)
có thể gợi ý viêm khớp dạng thấp (RA), nhưng có độ nhạy và độ đặc hiệu hạn chế. RF có thể xuất hiện trong các bệnh khác bao gồm hội chứng Sjögren, lupus ban đỏ hệ thống (SLE) và nhiều bệnh nhiễm trùng khác nhau. - Anti-CCP
có độ đặc hiệu cao nhưng độ nhạy hạn chế đối với viêm khớp dạng thấp. Nó cũng có thể xuất hiện trong các bệnh như viêm khớp vảy nến, lupus ban đỏ hệ thống, hội chứng Sjögren và viêm cơ viêm da. - Kháng thể đặc hiệu viêm cơ
thường được gọi là ‘blot viêm cơ’, do tính đặc hiệu cao đối với các bệnh viêm cơ tự miễn (IIM) như viêm da cơ. - Kháng thể kháng bào tương bạch cầu trung tính (ANCA)
xuất hiện dưới dạng bào tương (cANCA) hoặc quanh nhân (pANCA), và là các dấu ấn sinh học đặc trưng của viêm mạch máu. - Enzyme chuyển đổi angiotensin (ACE) và thụ thể interleukin-2 hòa tan (sIL2R)
là các dấu ấn sinh học được sử dụng trong đánh giá và theo dõi bệnh sarcoidosis. - Kết tủa huyết thanh
là các kháng thể IgG huyết thanh
chống lại các kháng nguyên đặc hiệu (ví dụ: vẹt hoặc ngỗng) và được sử dụng trong đánh giá
viêm phổi quá mẫn.
Bronchoalveolar lavage (BAL)
Rửa phế quản phế nang miễn dịch (BAL) là một thủ thuật chẩn đoán để thu thập dịch tiết đường hô hấp.
Kết quả BAL có giá trị hạn chế trong chẩn đoán UIP/IPF, ngoại trừ việc loại trừ các căn nguyên tiềm ẩn khác.
- Tăng lymphocyte trong dịch rửa phế quản phế nang (tức là số lượng tế bào >25%) rất có khả năng do bệnh phổi kẽ liên quan đến hình thành u hạt (ví dụ: viêm phổi quá mẫn hoặc độc tính thuốc), đặc biệt khi kèm theo tương bào và tiền sử phơi nhiễm phù hợp.
- Số lượng tế bào bạch cầu ái toan cao gợi ý bệnh phổi tăng bạch cầu ái toan tiềm ẩn.
- Đại thực bào phế nang chứa sắc tố thường được tìm thấy ở người hút thuốc, và có thể hỗ trợ chẩn đoán viêm tiểu phế quản hô hấp (RB-ILD) hoặc viêm phổi kẽ dạng bong vảy (DIP).
- Xuất huyết phế nang lan tỏa (DAH) sẽ tạo ra dịch hút có màu đỏ với nhuộm hemosiderin dương tính.
Pathology
Nếu sau khi đánh giá lâm sàng, chụp CT và các xét nghiệm chẩn đoán bổ sung vẫn chưa có chẩn đoán xác định, nhóm đa chuyên khoa (MDT) có thể quyết định cần thực hiện sinh thiết phổi.
Tuy nhiên, điều này phụ thuộc nhiều vào nguyện vọng của bệnh nhân, các bệnh đồng mắc và các lựa chọn điều trị hiện có, vì thủ thuật này có nguy cơ tương đối cao về biến chứng và tử vong.
Thường thực hiện sinh thiết phổi bằng phẫu thuật nội soi lồng ngực có hỗ trợ video (VATS), trong đó thông thường lấy ba mẫu từ mỗi thùy của phổi phải.
Một lựa chọn gần đây hơn là sinh thiết lạnh qua nội soi, tuy nhiên, hiệu suất thường không tối ưu so với sinh thiết phẫu thuật.
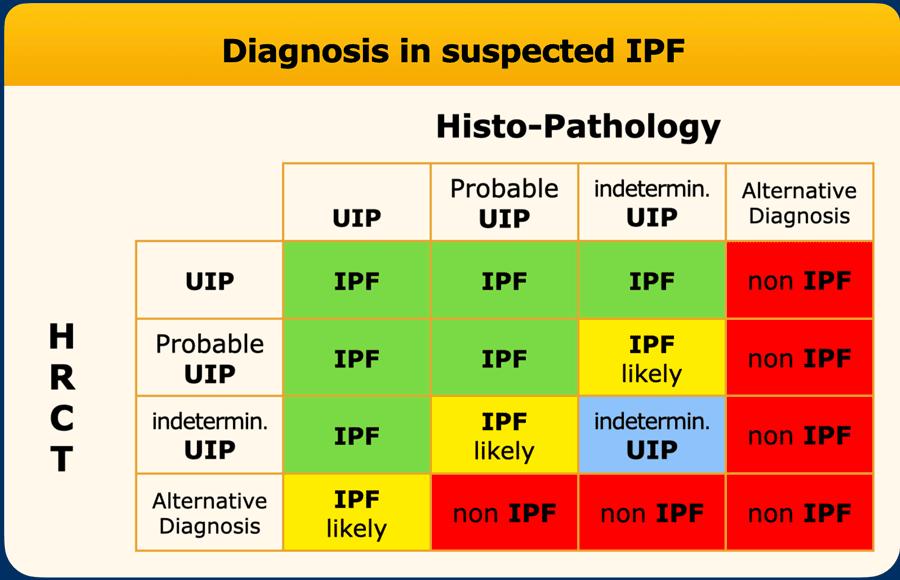
Chẩn đoán xác định IPF dựa trên các phát hiện trên HRCT kết hợp với mô bệnh học (bảng).
Treatment and follow-up
Bệnh nhân ILD thường được theo dõi bằng PFT và hình ảnh HRCT để đánh giá sự tiến triển của bệnh.
Tùy thuộc vào chẩn đoán cuối cùng, có thể áp dụng liệu pháp điều trị bằng thuốc.
Sự phân chia nhị phân của các lựa chọn điều trị là thuốc kháng xơ hóa (trong bệnh phổi xơ hóa nguyên phát như IPF) so với liệu pháp ức chế miễn dịch (trong bệnh phổi xơ hóa qua trung gian miễn dịch như HP mạn tính hoặc ILD liên quan đến CTD).
Thuốc có thể được kết hợp với việc chấm dứt tiếp xúc với kháng nguyên hoặc thuốc gây độc phổi, cai thuốc lá, phục hồi chức năng phổi, v.v.
Ghép phổi có thể là nỗ lực cuối cùng, nếu có thể thực hiện được.