Đặc điểm tổn thương tuyến thượng thận
Ngày xuất bản
Bản cập nhật của bài viết này với các ngưỡng giá trị mới sẽ sớm được công bố.
Các tổn thương tuyến thượng thận rất phổ biến.
Nhiều tổn thương trong số này được phát hiện tình cờ và được gọi là u tình cờ (incidentaloma).
U tình cờ tuyến thượng thận được định nghĩa là một khối > 1 cm được phát hiện trên các phương tiện chẩn đoán hình ảnh không được thực hiện vì nghi ngờ bệnh lý tuyến thượng thận.
Hầu hết các u tình cờ này là u tuyến lành tính không hoạt động chức năng, ngay cả ở những bệnh nhân có bệnh ác tính đã biết trước đó.
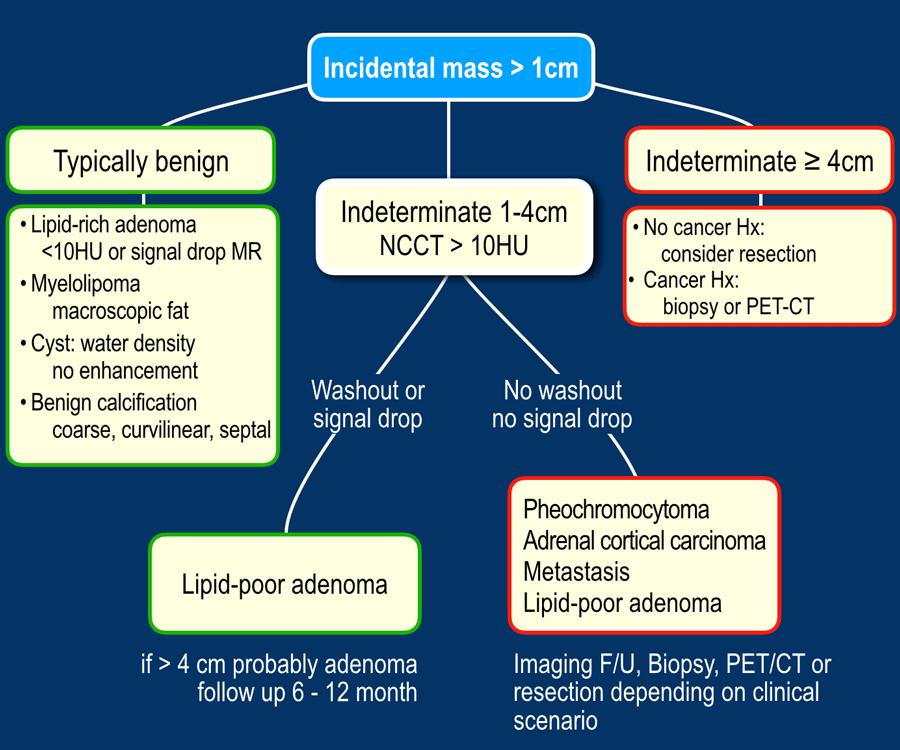
Trong bài viết này, chúng tôi sẽ thảo luận về việc đánh giá và xử trí các khối tuyến thượng thận bằng cách phân chia chúng thành:
- Các tổn thương có đặc điểm hình ảnh lành tính
- Các tổn thương chưa xác định từ 1-4 cm
- Các tổn thương chưa xác định > 4 cm
Tiếp Cận Có Hệ Thống
U tuyến thượng thận tình cờ (incidentaloma) là tổn thương thường gặp, xuất hiện trong khoảng 3% các ca chụp CT bụng, tỷ lệ này tăng lên đến 10% ở bệnh nhân cao tuổi [1,2,3].
Trước tiên, cần xác định xem tổn thương có đặc điểm hình ảnh điển hình của lành tính hay là không xác định.
Nếu không xác định, thực hiện CT đánh giá washout hoặc MRI để xem liệu đó có phải là u tuyến nghèo lipid hay không.
Nếu không phải u tuyến, cần lựa chọn giữa các phương án: theo dõi, PET-CT, sinh thiết hoặc phẫu thuật cắt bỏ.
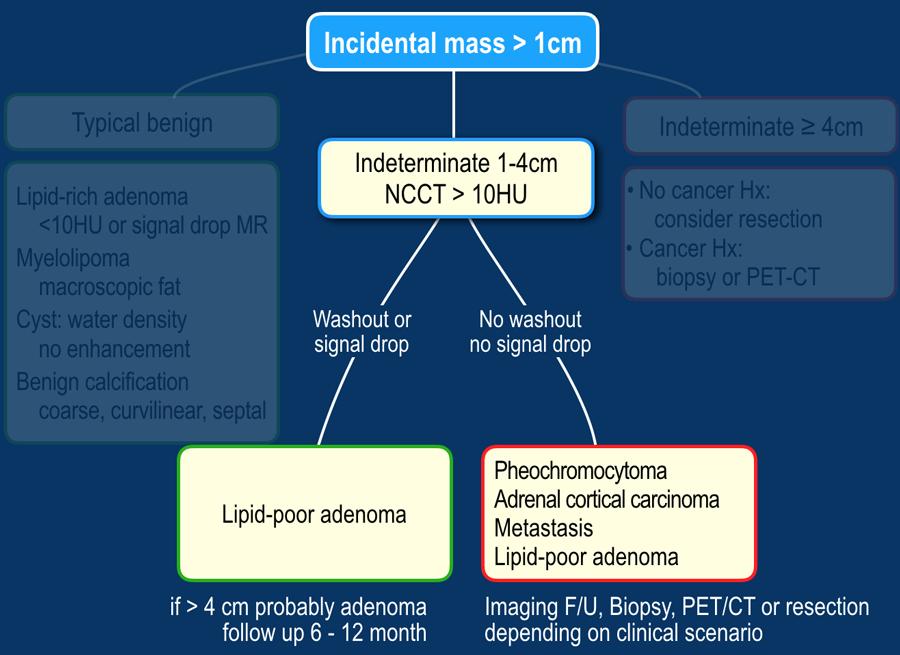
Khi phát hiện u tuyến thượng thận tình cờ, áp dụng các bước sau:
- Nếu tổn thương có đặc điểm hình ảnh điển hình của lành tính, không cần theo dõi.
Điều này bao gồm các tổn thương ổn định lâu dài khi so sánh với hình ảnh trước đó. - Nếu tổn thương không xác định và có đường kính 1-4 cm:
- Các tổn thương 1-2 cm ở bệnh nhân không có tiền sử ung thư có khả năng lành tính. Có thể cân nhắc theo dõi sau 12 tháng.
- Đối với tất cả các tổn thương không xác định còn lại, thực hiện CT tuyến thượng thận chuyên biệt hoặc MRI để chẩn đoán u tuyến nghèo lipid.
Các tổn thương này không cần theo dõi thêm. - Nếu tổn thương không phải u tuyến nghèo lipid, bước tiếp theo phụ thuộc vào bối cảnh lâm sàng. Nếu bệnh nhân có tiền sử ung thư, cân nhắc PET hoặc sinh thiết.
Nếu không, cân nhắc theo dõi hoặc phẫu thuật cắt bỏ.
- Nếu tổn thương không xác định và có đường kính ≥ 4 cm:
- Không có tiền sử ung thư, cân nhắc phẫu thuật cắt bỏ do khả năng là ung thư vỏ thượng thận. Không sinh thiết.
- Nếu có tiền sử ung thư, cân nhắc PET hoặc sinh thiết.
Chúng tôi sẽ lần lượt thảo luận từng khả năng này.
Các tổn thương thường gặp lành tính
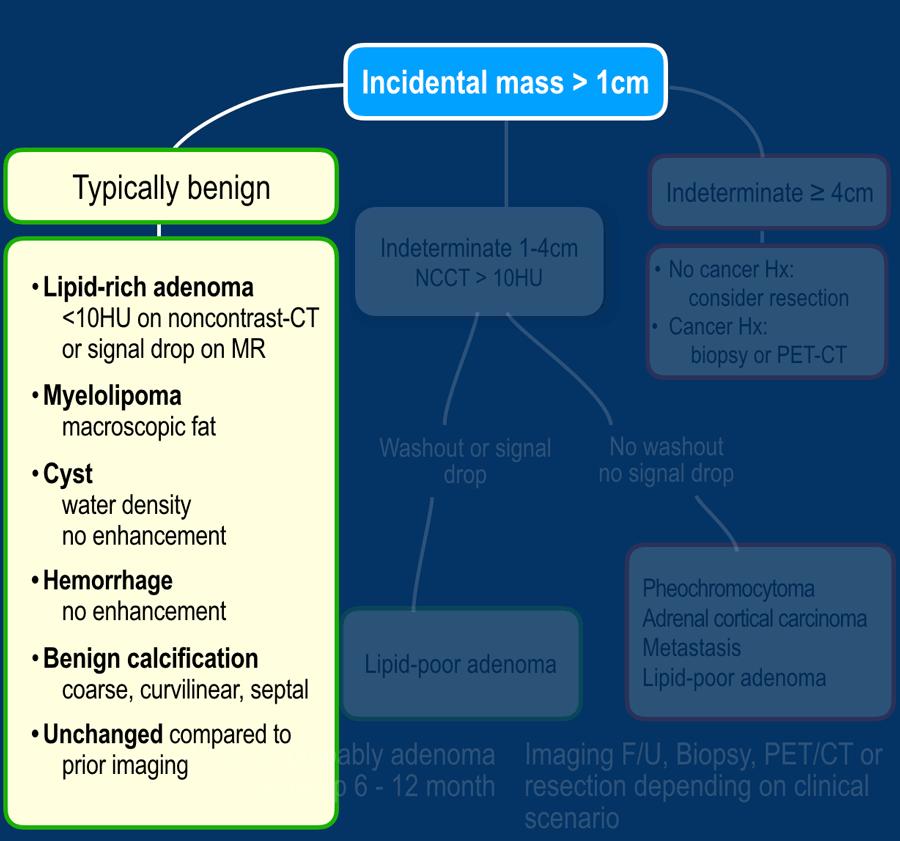
Nhiều tổn thương tuyến thượng thận có thể được phân loại là thường gặp lành tính và không cần theo dõi (bảng):
- U tuyến giàu lipid
- U tủy mỡ (Myelolipoma)
- Nang
- Xuất huyết (có tiền sử phù hợp, ví dụ: chấn thương hoặc bệnh nặng)
- Các tổn thương có vôi hóa lành tính
- Các tổn thương không thay đổi trong thời gian dài (> 6-12 tháng) (+ không có tiền sử ung thư)
- Các tổn thương không ngấm thuốc
‘Không ngấm thuốc’ được định nghĩa là sự chênh lệch nhỏ hơn 10HU giữa CT không tiêm và CT có tiêm thuốc cản quang.
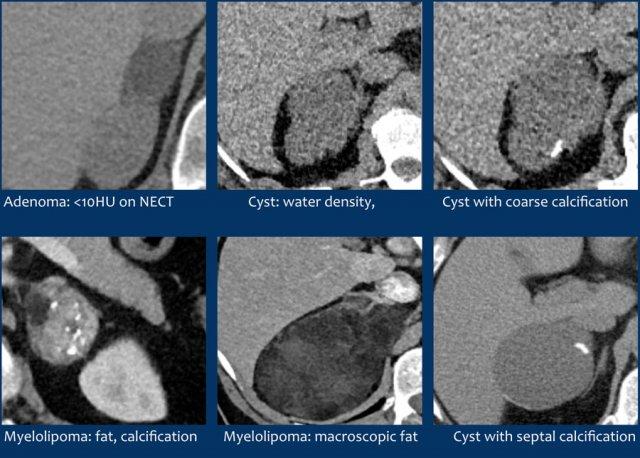
Dưới đây là một số ví dụ về các tổn thương thường gặp lành tính.
U tuyến giàu lipid
70% u tuyến chứa nhiều mỡ nội bào và sẽ có tỷ trọng thấp trên CT không tiêm thuốc cản quang [4,5].
Tỷ trọng bằng hoặc dưới 10 HU được coi là tiêu chuẩn chẩn đoán u tuyến giàu lipid.
Sử dụng ngưỡng an toàn 10HU trên CT không tiêm thuốc cho độ nhạy 70-79% và độ đặc hiệu cao 96-98% trong chẩn đoán u tuyến [5-7].
30% u tuyến thượng thận không chứa đủ lipid nội bào để có tỷ trọng dưới 10 HU và không thể phân biệt với các tổn thương không phải u tuyến trên CT không tiêm thuốc cản quang.
Các u tuyến này được gọi là u tuyến nghèo lipid.
Chúng có thể được chẩn đoán bằng CT tuyến thượng thận chuyên biệt để đánh giá tốc độ thải thuốc nhanh.
Các u tuyến nghèo lipid này sẽ được thảo luận trong chương về các tổn thương chưa xác định.
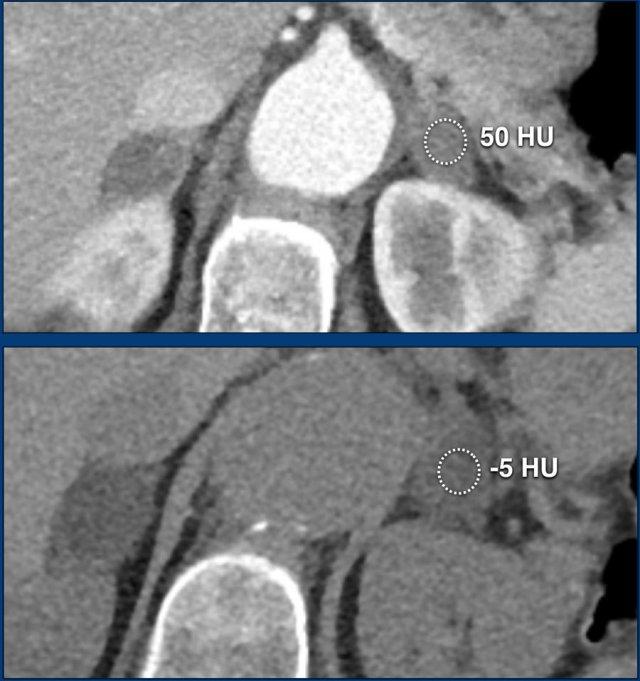
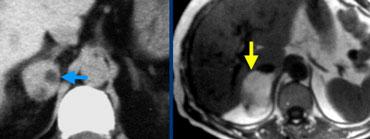
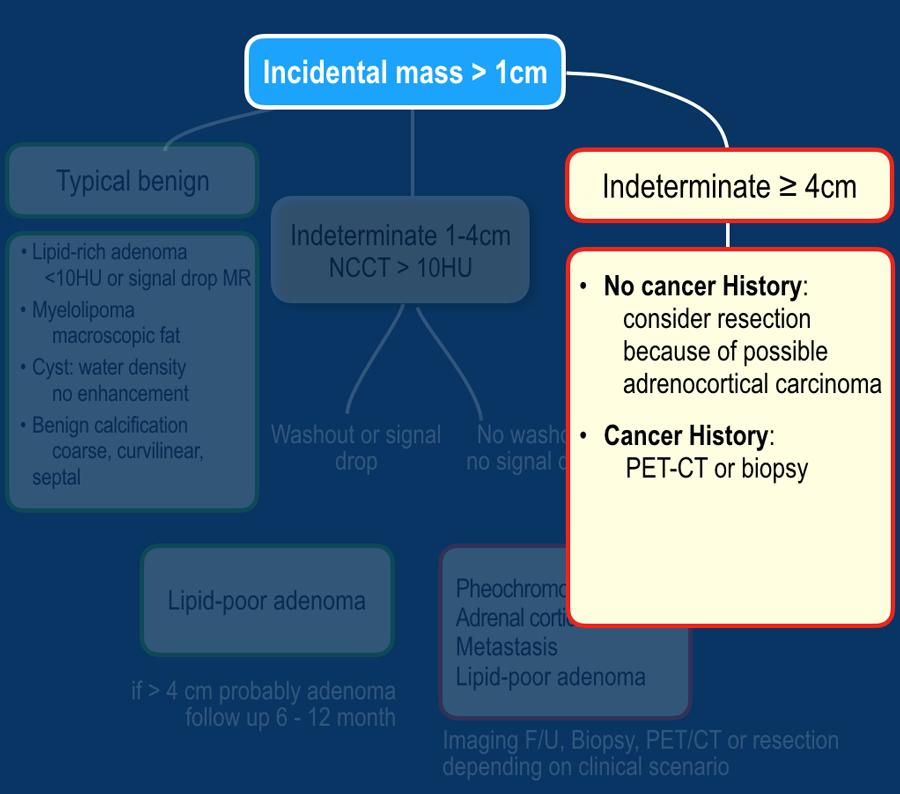
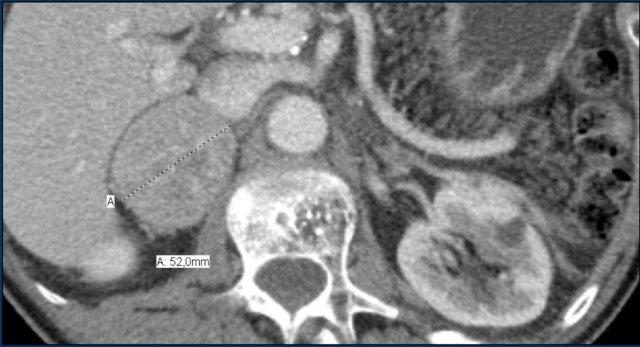
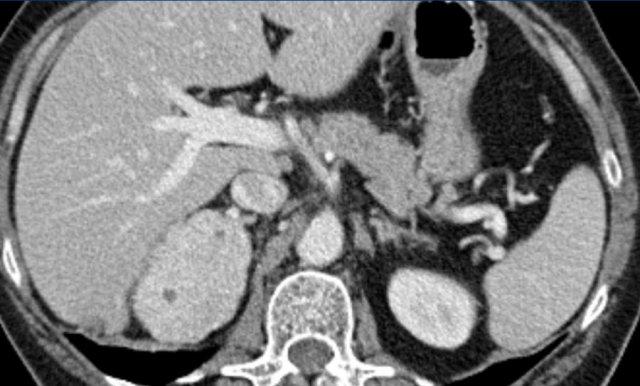
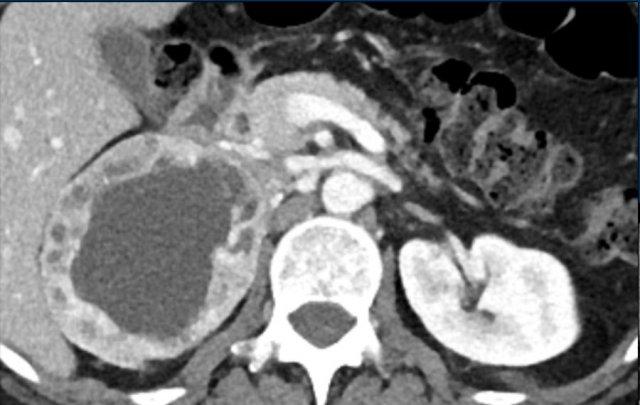
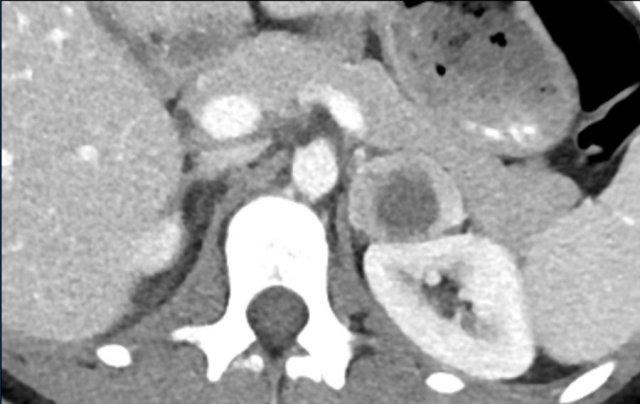
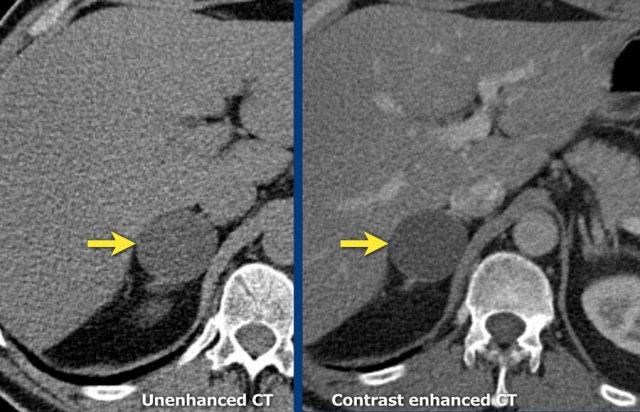
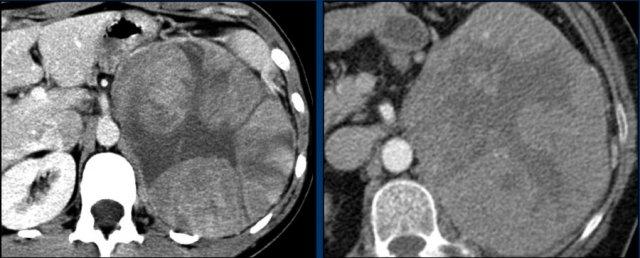
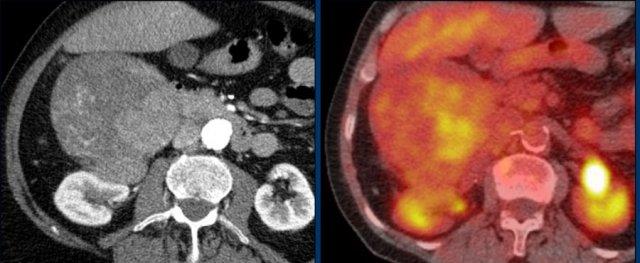
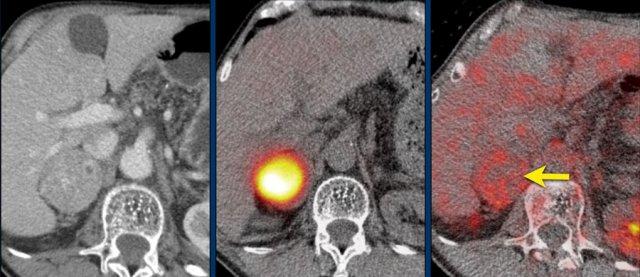
Các hình ảnh cho thấy u tình cờ tuyến thượng thận hai bên được phát hiện ở bệnh nhân 64 tuổi được chụp CT để phân tích phình động mạch chủ bụng.
Hình chụp pha động mạch cho thấy các tổn thương hai bên với tỷ trọng 50 HU.
Trên CT không tiêm thuốc thực hiện vài ngày sau, tỷ trọng ở cả hai tuyến thượng thận đều dưới 10 HU, xác nhận đây là các u tuyến giàu lipid.
Nang
Nang đơn thuần là tổn thương bờ rõ, tỷ trọng nước và không ngấm thuốc cản quang.
Nang có thành mỏng và có thể có các vách mỏng.
Có thể là nang nội mô hoặc giả nang, đây là các loại phổ biến nhất, hoặc nang biểu mô thực sự hay nang ký sinh trùng (cả hai đều hiếm gặp) [5].
Giả nang có thể có thành dày hơn.
Xuất huyết hoặc mảnh vụn có thể làm tăng tỷ trọng bên trong.
Cả khối u lành tính và ác tính đều có thể có thoái hóa dạng nang và hoại tử.
Trong những trường hợp đó, các phép đo tỷ trọng không đáng tin cậy.
Các đặc điểm gợi ý khối u nền có thể là thành không đều dày từ 5 mm trở lên và ngấm thuốc ở thành, vách hoặc thành phần đặc [5].
Các tổn thương có vôi hóa lành tính
Vôi hóa thô, dạng tròn, ngoại vi hoặc theo vách thường gặp trong lành tính và có thể thấy trong:
- U tuyến
- U tủy mỡ (Myelolipoma)
- Chấn thương
- Nhiễm trùng u hạt
Vôi hóa hai bên cũng gợi ý nguồn gốc lành tính.
Vôi hóa dạng chấm, loạn dưỡng và không đều không phải là đặc điểm thường gặp lành tính và có thể thấy trong:
- Ung thư vỏ thượng thận
- Di căn tuyến thượng thận
U tủy mỡ (Myelolipoma)
U tủy mỡ là các khối u lành tính cấu thành từ các thành phần tủy xương.
Thông thường chúng dễ nhận biết trên CT hoặc MRI vì chứa các vùng mỡ đại thể.
Vôi hóa gặp trong 24% các trường hợp.
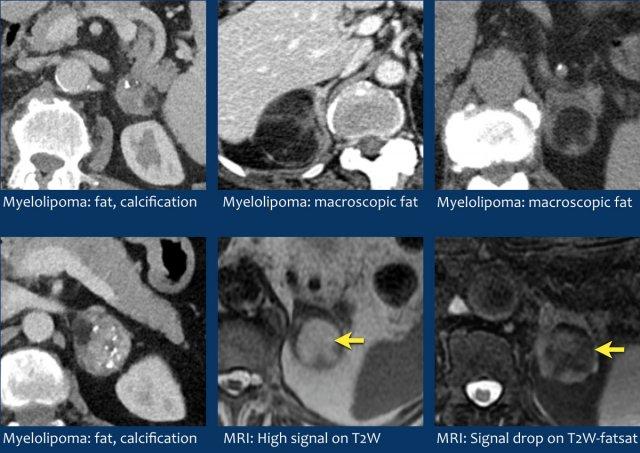
Khối tuyến thượng thận thấy trên CT ở đây chứa mỡ đại thể, đặc hiệu cho chẩn đoán u tủy mỡ.
Bên phải là một trường hợp khác với tăng tín hiệu trên chuỗi xung T1W cho thấy mỡ đại thể trong u tủy mỡ.
Hình ảnh CT của một khối tuyến thượng thận khác chủ yếu cấu thành từ mỡ đại thể.
Chẩn đoán: u tủy mỡ.
Tổn thương chưa xác định 1-4 cm
Nhiều tổn thương tuyến thượng thận không thể được chẩn đoán chắc chắn là u tuyến giàu lipid hay một thực thể lành tính khác, do tỷ trọng quá cao trên CT không tiêm thuốc cản quang, hoặc do chỉ có hình ảnh CT có tiêm thuốc cản quang để đánh giá.
Các tổn thương này được gọi là tổn thương chưa xác định.
Nhóm này bao gồm 30% u tuyến nghèo lipid.
Để xác định một tổn thương có phải là u tuyến nghèo lipid hay không, có thể thực hiện CT đánh giá độ thải thuốc (washout) và tìm kiếm dấu hiệu thải thuốc nhanh, hoặc chụp MRI và tìm kiếm sự giảm tín hiệu trên chuỗi xung đảo pha (out-of-phase).
Độ thải thuốc tuyến thượng thận (Adrenal Washout)
U tuyến, cả loại giàu lipid lẫn nghèo lipid, đều thải thuốc cản quang nhanh chóng.
Các tổn thương không phải u tuyến, ví dụ như di căn, thường ngấm thuốc nhanh nhưng thải thuốc chậm hơn.
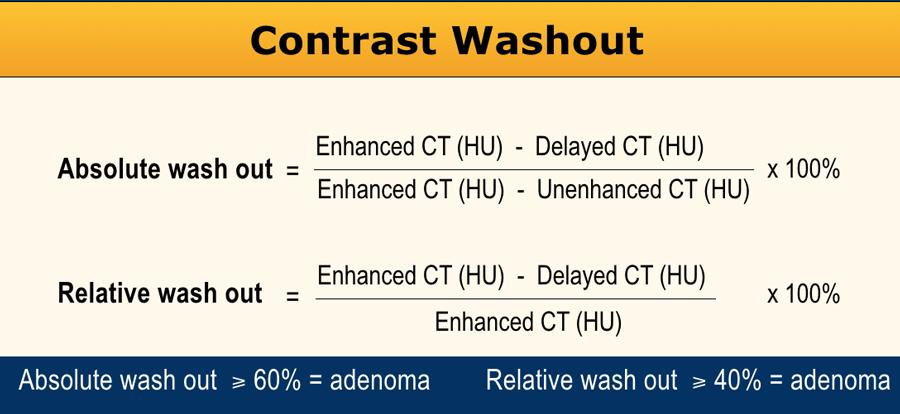
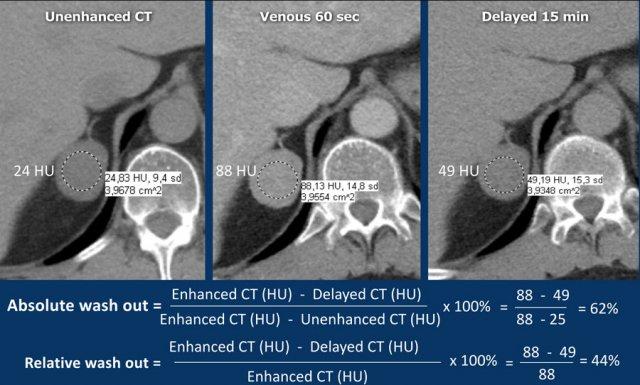
Độ thải thuốc tuyệt đối
Quy trình CT đánh giá độ thải thuốc tuyến thượng thận chuyên biệt bao gồm: pha không tiêm thuốc, pha tiêm thuốc cản quang với thì chụp muộn 60-90 giây, và pha chụp muộn tại thời điểm 15 phút.
Vùng quan tâm (ROI) cần bao phủ ít nhất 2/3 diện tích tổn thương để đảm bảo tính đại diện trong đánh giá.
Độ thải thuốc tuyệt đối ⩾ 60% là bằng chứng xác định u tuyến [5,6,8].
Độ thải thuốc tương đối
Nếu tổn thương tuyến thượng thận được phát hiện trên pha tiêm thuốc cản quang trong khi bệnh nhân vẫn còn trên bàn chụp, có thể thực hiện thêm một lần chụp tuyến thượng thận tại thời điểm 15 phút sau khi tiêm thuốc và tính toán độ thải thuốc tương đối.
Độ thải thuốc tương đối ⩾ 40% là bằng chứng xác định u tuyến [5,6,8].
Những lưu ý khi đánh giá độ thải thuốc tuyến thượng thận
Các ngoại lệ quan trọng của quy tắc thải thuốc là do các khối u có tỷ lệ phần trăm thải thuốc tuyệt đối và tương đối nằm trong ngưỡng của u tuyến, theo thứ tự giảm dần về tần suất gặp:
- Di căn tuyến thượng thận từ các khối u nguyên phát tăng sinh mạch như ung thư biểu mô tế bào thận (RCC) và ung thư biểu mô tế bào gan (HCC) [17]
- U tủy thượng thận (Pheochromocytoma)
- Ung thư biểu mô vỏ thượng thận [10]
Công cụ tính độ thải thuốc (Washout Calculator)
Nhấn vào đây để truy cập Công cụ tính đặc điểm tuyến thượng thận.
U tuyến nghèo lipid
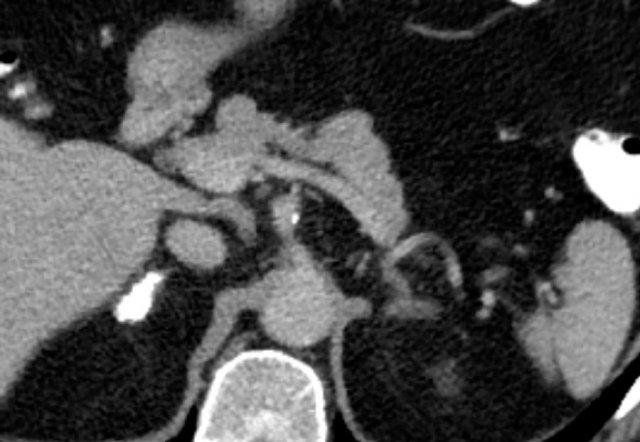
Các hình ảnh cho thấy một tổn thương chưa xác định trên CT không tiêm thuốc cản quang (tỷ trọng 24 HU).
Độ thải thuốc tuyệt đối ở bệnh nhân này là 62%.
Điều này có nghĩa là tổn thương là u tuyến nghèo lipid.
Thông thường, u tuyến có đặc điểm ngấm thuốc khác với các tổn thương ác tính.
Trên CT tiêm thuốc cản quang ở thì 60 giây, hầu hết u tuyến ngấm thuốc nhẹ, trong khi các khối u ác tính và u tủy thượng thận ngấm thuốc mạnh.
Tuy nhiên, sự chồng lấp quá nhiều về mức độ ngấm thuốc không cho phép phân biệt chính xác giữa các tổn thương này, và đó là lý do tại sao chúng ta cần thực hiện CT đánh giá độ thải thuốc.
MRI chuỗi xung đảo pha (Out-of-phase imaging)
U tuyến nghèo lipid cũng có thể được chẩn đoán bằng chuỗi xung đảo pha.
Các u này chứa đủ lượng mỡ vi thể để gây ra sự giảm tín hiệu trên ảnh đảo pha so với ảnh đồng pha, do xảo ảnh dịch chuyển hóa học.
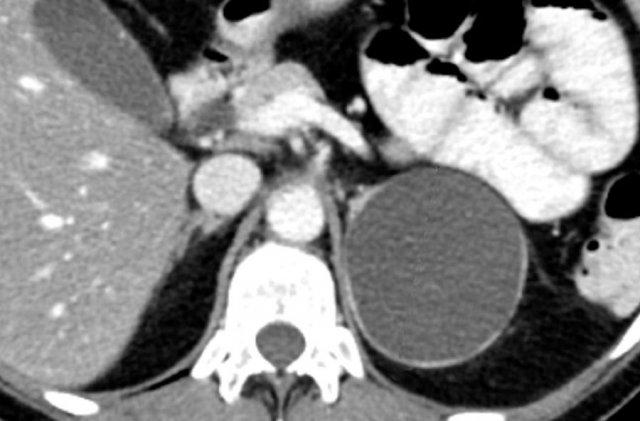
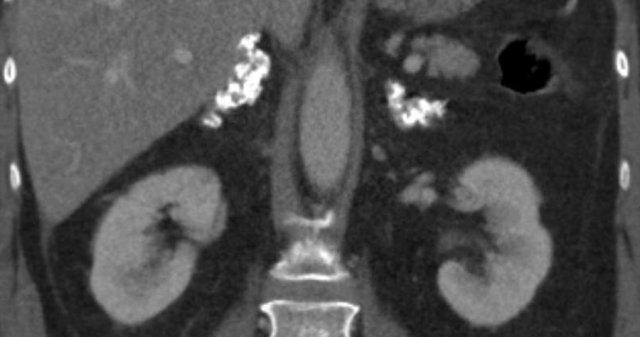
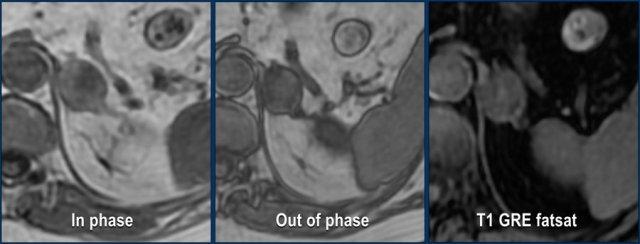
Đây là hình ảnh của bệnh nhân nữ 65 tuổi, phát hiện tình cờ khối tuyến thượng thận phải trên siêu âm ổ bụng được thực hiện vì sỏi thận.
Sự hiện diện của mỡ vi thể được chứng minh bởi sự giảm tín hiệu trên ảnh đảo pha.
Bệnh nhân được theo dõi trong 2 năm do tổn thương hơi không đồng nhất và có kích thước 5,2 cm.
Tổn thương không thay đổi kích thước và không có hoạt động nội tiết.
Tổn thương được chẩn đoán là u tuyến nghèo lipid.
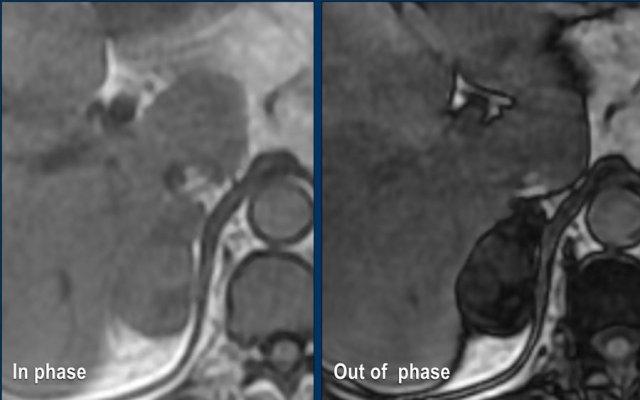
MRI được thực hiện cho tổn thương tình cờ tuyến thượng thận trái phát hiện trên CT không tiêm thuốc và pha động mạch ở bệnh nhân nam 61 tuổi có phình động mạch chủ bụng.
Trên CT không tiêm thuốc, tỷ trọng là 18 HU.
Ảnh T1 đảo pha cho thấy sự giảm tín hiệu không đồng nhất kín đáo so với ảnh đồng pha.
Lưu ý rằng chuỗi xung T1 có xóa mỡ không có giá trị trong việc phát hiện mỡ nội bào vi thể.
Tiếp tục xem các hình ảnh tiếp theo.
Vùng tăng tín hiệu trung tâm kín đáo trên chuỗi xung T1 xóa mỡ cũng tăng tín hiệu trên chuỗi xung T2W và không ngấm thuốc tương phản từ trên ảnh sau tiêm.
Sau khi so sánh với các hình ảnh CT trước đó từ nhiều năm trước, tổn thương được xác định là u tuyến phát triển chậm với xuất huyết nội u mới xảy ra.
Tổn thương không xác định > 4 cm
Đường kính lớn nhất của khối tuyến thượng thận có giá trị tiên lượng ác tính.
Đặc biệt, các tổn thương > 4 cm có khả năng cao là di căn hoặc ung thư biểu mô vỏ thượng thận.
Kích thước khối tuyến thượng thận còn quan trọng vì hai lý do khác.
Tiên lượng chung tốt hơn đối với ung thư biểu mô vỏ thượng thận kích thước nhỏ, và các khối u nhỏ hơn cũng dễ cắt bỏ hơn bằng các kỹ thuật phẫu thuật xâm lấn tối thiểu.
Do đó, khuyến cáo đối với khối tuyến thượng thận không xác định có kích thước > 4 cm và không có tiền sử ung thư là phẫu thuật cắt bỏ – trong hầu hết các trường hợp không cần sinh thiết – nhằm điều trị kịp thời ung thư biểu mô vỏ thượng thận nguyên phát có thể xảy ra [3,9].
Các trường hợp tiếp theo là ví dụ về các tổn thương không xác định > 4 cm.
Tất cả đều được phát hiện tình cờ ở những bệnh nhân không có tiền sử ung thư.
Tất cả các chẩn đoán đều được xác nhận bằng mô bệnh học và cho thấy sự đa dạng của cả khối u lành tính lẫn ác tính.
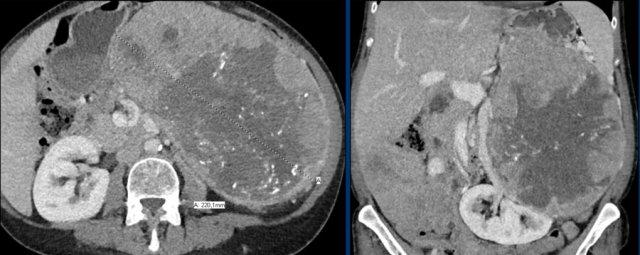
Hình ảnh cho thấy một khối không đồng nhất, bờ không rõ, kích thước lớn hơn 4 cm.
Có vùng trung tâm ngấm thuốc kém, nhiều khả năng là do hoại tử trung tâm.
Trong trường hợp cụ thể này, sinh thiết đã được thực hiện và cho thấy ung thư biểu mô tuyến, có thể xuất phát từ ung thư phổi nguyên phát.
Tuy nhiên, điều đáng ngạc nhiên là phân tích hình ảnh toàn diện, bao gồm cả FDG PET-CT, không phát hiện được khối u nguyên phát.
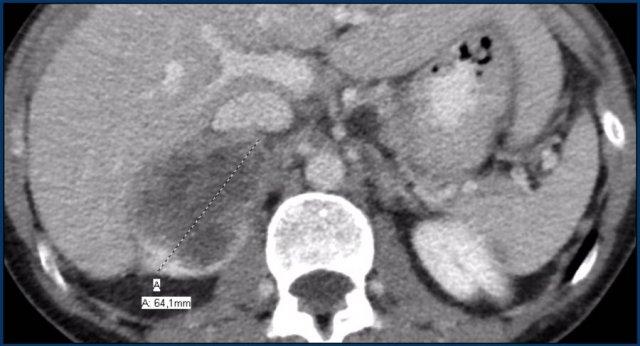
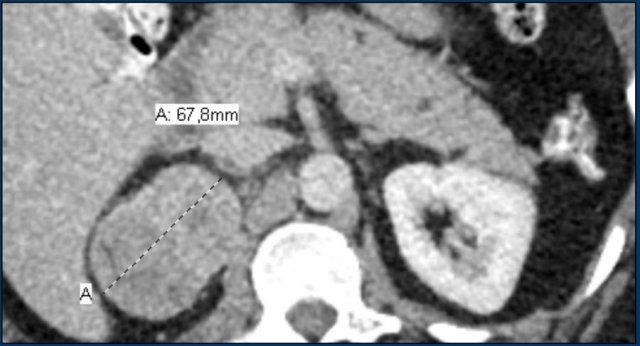
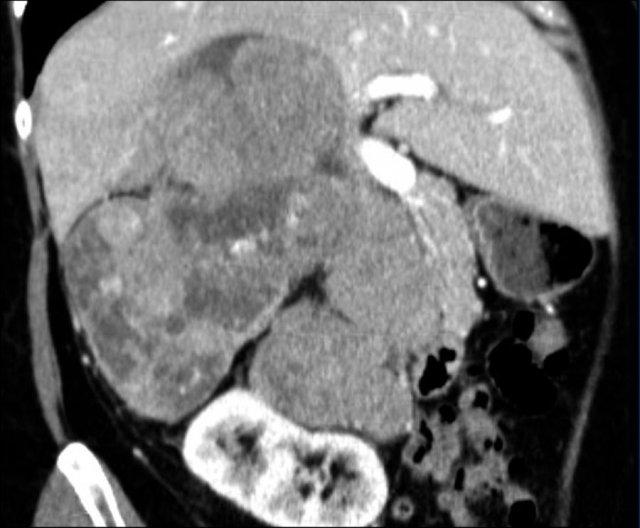
Hình ảnh cho thấy một tổn thương ngấm thuốc không đồng nhất, bờ tương đối rõ, kích thước 67 mm.
Sau phẫu thuật cắt bỏ, tổn thương được xác định là ung thư biểu mô vỏ thượng thận.
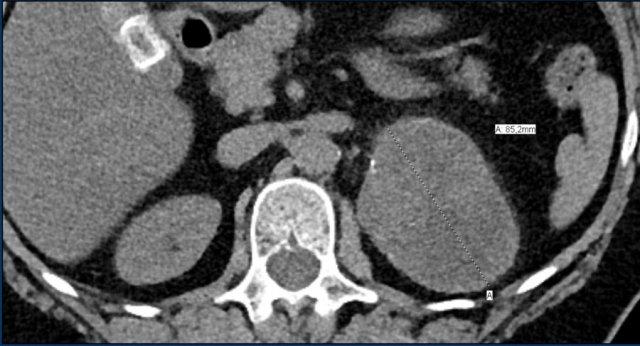
Hình ảnh cho thấy một tổn thương không xác định kích thước lớn với tỷ trọng không đồng nhất và vỏ vôi hóa một phần.
Sinh thiết cho thấy u cơ trơn tuyến thượng thận.
Tổn thương đã được phẫu thuật cắt bỏ.
Đây là tổn thương không xác định, ngấm thuốc không đồng nhất, bờ tương đối rõ.
Tổn thương được xác định là u tủy thượng thận (pheochromocytoma).
Tổn thương tuyến thượng thận ngấm thuốc mạnh kích thước 7 cm với các ổ nang nhỏ.
Tổn thương được phẫu thuật cắt bỏ do kích thước lớn và đặc điểm hình ảnh không xác định.
Kết quả mô bệnh học xác định đây là u tuyến (adenoma).
Các khối u tuyến thượng thận đặc hiệu
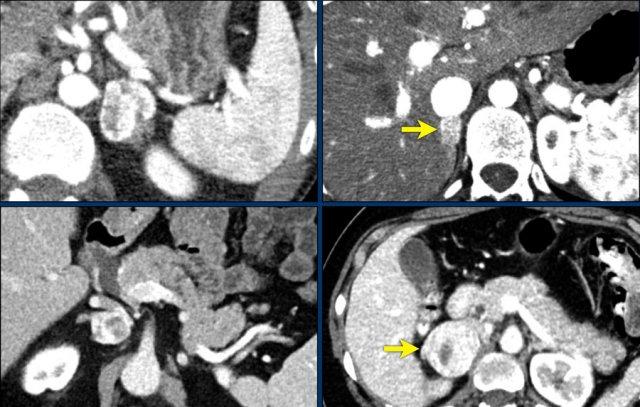
U tủy thượng thận (Pheochromocytoma): ngấm thuốc mạnh trong cả 4 trường hợp, kể cả các khối u nhỏ hơn
U tủy thượng thận (Pheochromocytoma)
U tủy thượng thận là các khối u hiếm gặp, có nguồn gốc từ tủy thượng thận.
Thông thường, các khối u có kích thước lớn hơn 3 cm khi được phát hiện.
Các khối u không chức năng thường có kích thước lớn hơn các khối u có chức năng.
Một u tủy thượng thận điển hình sẽ có tỷ trọng trên CT không tiêm thuốc >10 HU, hoặc cao hơn trong trường hợp có xuất huyết.
Khối u có tính chất giàu mạch máu, dẫn đến ngấm thuốc mạnh, nhưng khác với u tuyến (adenoma), chúng thường có thải trừ thuốc chậm [4,5].
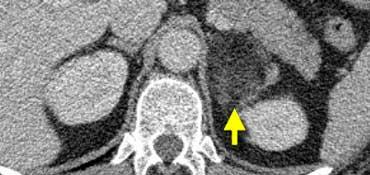
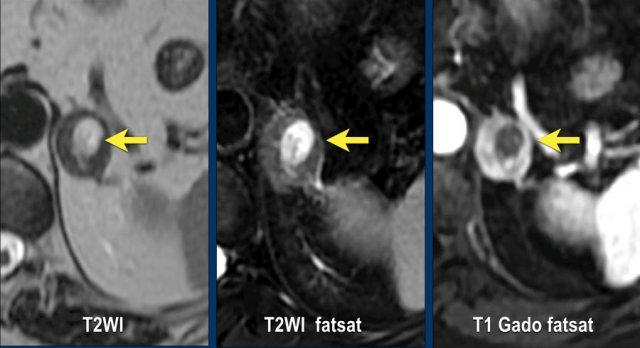
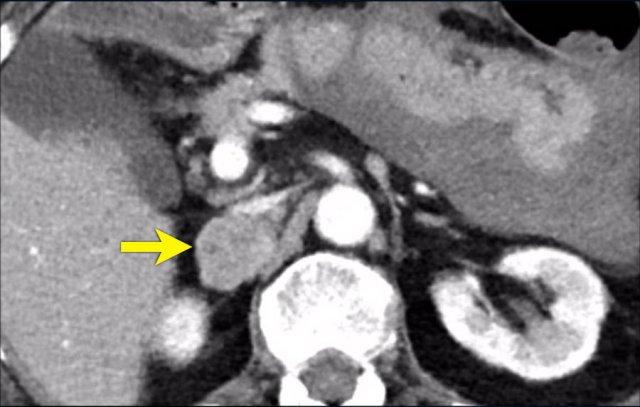
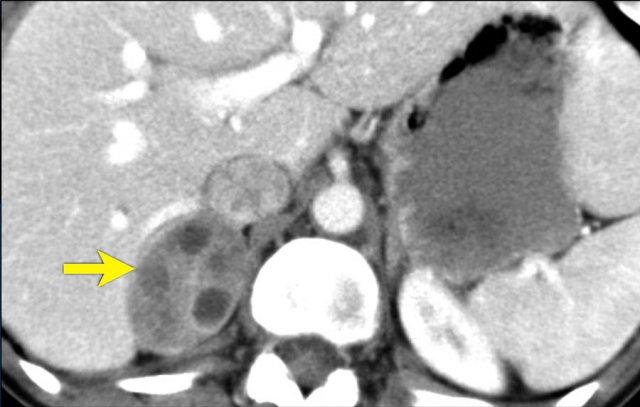
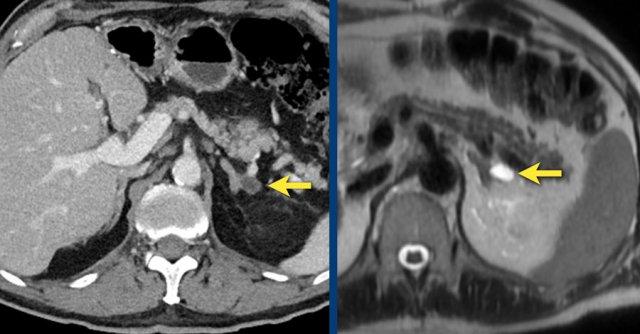
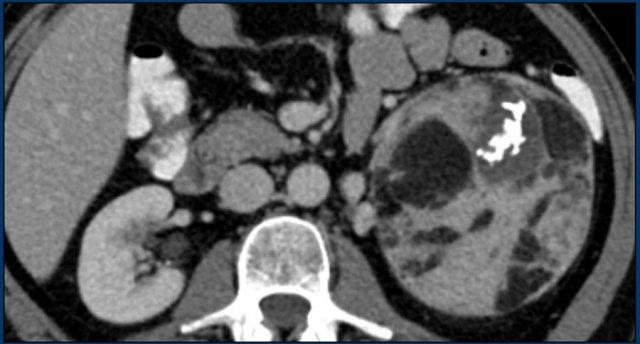
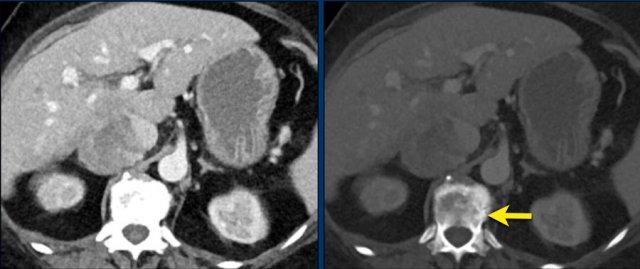
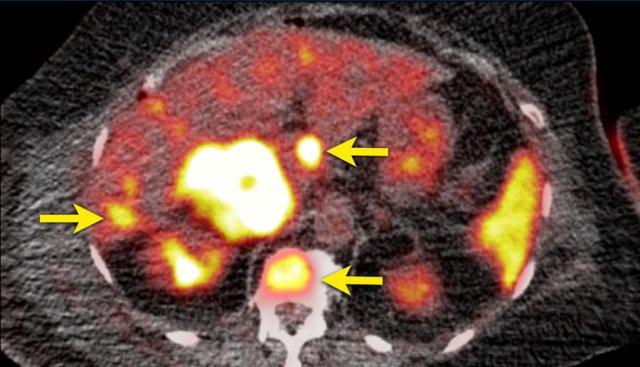
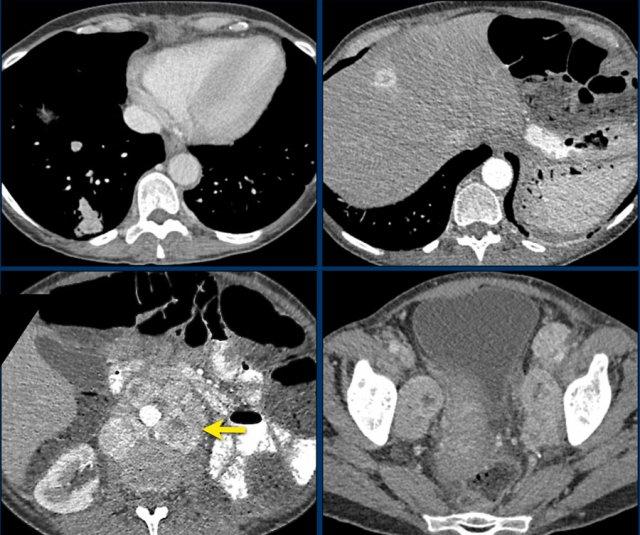
Trong 10% trường hợp, u tủy thượng thận có vôi hóa và thường có nhiều nang (mũi tên vàng).
Hình ảnh này cho thấy một trường hợp u tủy thượng thận khác với nhiều nang.
Các khối u lớn hơn có xu hướng xuất huyết và hoại tử, ngay cả khi chúng là lành tính.
U tủy thượng thận được mệnh danh là “tắc kè hoa trên hình ảnh học” vì nhiều đặc điểm hình ảnh chồng lấp với các khối u khác [5].
Dấu hiệu kinh điển được gọi là “dấu bóng đèn” (light bulb sign), biểu hiện bằng tín hiệu cao đồng nhất trên chuỗi xung T2W, được ghi nhận trong 65% trường hợp [4].
Những bẫy hình ảnh (Imaging pitfalls)
- Tỷ trọng < 10 HU trên CT không tiêm thuốc chỉ được mô tả trong các báo cáo ca lâm sàng đơn lẻ.
- Cả thành phần mỡ vi thể và đại thể đều đã được ghi nhận.
- Một số ít u tủy thượng thận có thể bị chẩn đoán nhầm là u tuyến nghèo lipid do có tỷ lệ thải trừ thuốc tương đối và tuyệt đối tương tự.
- Lên đến 30% u tủy thượng thận có thể biểu hiện tín hiệu T2 thấp.
Do những bẫy hình ảnh này, chẩn đoán u tủy thượng thận dựa trên sự kết hợp các đặc điểm hình ảnh và thường được bổ sung bằng kết quả hình ảnh y học hạt nhân cùng xác nhận sinh hóa.
Khối u “10%”?
U tủy thượng thận từng được gọi là “khối u 10%” vì người ta cho rằng 10% là ác tính, 10% hai bên, 10% có tính gia đình, 10% ngoài tuyến thượng thận và 10% xảy ra ở trẻ em.
Tuy nhiên, hiện nay đã rõ ràng rằng thực tế có hơn 30% u tủy thượng thận và u cận hạch (paraganglioma) là di truyền [18].
Hơn nữa, tỷ lệ các khối u hai bên, ngoài tuyến thượng thận, ở trẻ em hoặc ác tính khác nhau tùy theo từng hội chứng di truyền cụ thể [18].
Các hội chứng gia đình liên quan bao gồm đa u tuyến nội tiết (MEN) type IIA/B, von Hippel-Lindau, u xơ thần kinh type I, u cận hạch gia đình do đột biến gen SDH, hội chứng Sturge-Weber và bộ ba Carney (Carney triad) [5, 18].
10 – 49% u tủy thượng thận được phát hiện tình cờ ở bệnh nhân không có triệu chứng.
Do đó, bác sĩ chẩn đoán hình ảnh cần có ngưỡng thấp khi xem xét chẩn đoán u tủy thượng thận.
Chẩn đoán sinh hóa được thực hiện bằng cách đo metanephrine tự do trong huyết tương hoặc metanephrine phân đoạn trong nước tiểu [2,18].
Cần tránh sinh thiết không cần thiết và có thể gây nguy hiểm.
U tủy mỡ tuyến thượng thận (Myelolipoma)
U tủy mỡ tuyến thượng thận là các khối u lành tính, tương đối hiếm gặp (0,08-0,2%), chứa các thành phần tủy xương và mỡ trưởng thành với tỷ lệ thay đổi.
U tủy mỡ thường không có triệu chứng, trừ khi kích thước rất lớn (do hiệu ứng khối) hoặc có chảy máu [5].
Sự hiện diện của mỡ đại thể giúp nhận diện dễ dàng trên CT hoặc MRI.
Tỷ trọng trên CT không tiêm thuốc sẽ thấp hơn 0 HU rõ rệt.
Trên MRI, các phần mỡ sẽ tăng tín hiệu trên chuỗi xung T1W không bão hòa mỡ và mất tín hiệu trên chuỗi xung T1 hoặc T2W có bão hòa mỡ.
Vôi hóa được ghi nhận trong khoảng 24% trường hợp.
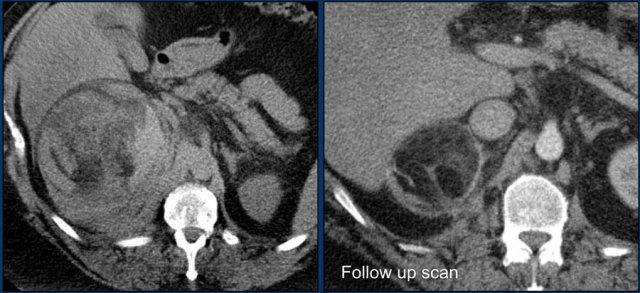
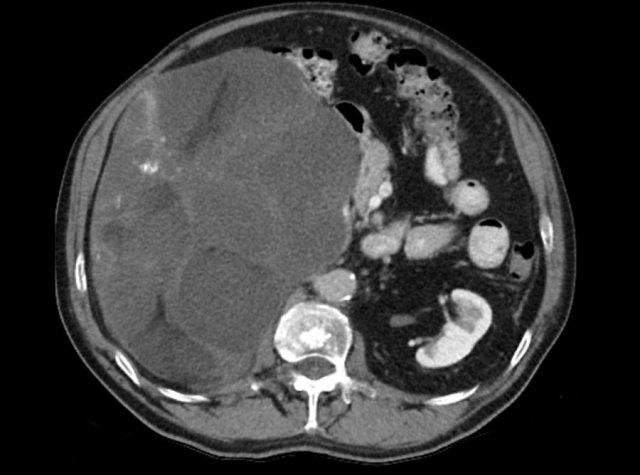
Hình ảnh cắt ngang và cắt vành cho thấy u tủy mỡ lớn bên phải kèm chảy máu.
Hình ảnh bên phải là phim chụp theo dõi.
Nang tuyến thượng thận
Đây là hình ảnh một nang nhỏ được quan sát trên CT và trên chuỗi xung T2W.
Hình ảnh CT không tiêm và có tiêm thuốc cản quang của một nang tuyến thượng thận.
Nang có thành mỏng, đồng nhất và không ngấm thuốc.
Ung thư vỏ thượng thận (Adrenocortical carcinoma)
Ung thư vỏ thượng thận (ACC) là các khối u ác tính hiếm gặp với tỷ lệ mắc khoảng 1-2 trường hợp trên một triệu dân mỗi năm [5].
60% ACC có chức năng nội tiết.
Hội chứng Cushing đơn thuần hoặc hội chứng Cushing kết hợp nam hóa là biểu hiện lâm sàng thường gặp nhất.
Nam hóa, nữ hóa hoặc cường aldosterone đơn thuần là hiếm gặp (< 10%).
Bệnh nhân ung thư vỏ thượng thận không chức năng thường biểu hiện các triệu chứng bụng như buồn nôn, nôn, đầy bụng, đau hông hoặc đau lưng do kích thước khối u lớn.
Ung thư vỏ thượng thận có thể là thể tản phát hoặc liên quan đến các hội chứng di truyền, bao gồm MEN1, hội chứng Lynch, hội chứng Beckwith-Wiedemann và hội chứng Li-Fraumeni.
Đỉnh tỷ lệ mắc xảy ra ở trẻ nhỏ và ở thập kỷ thứ tư và thứ năm của cuộc đời [5].
Các đặc điểm hình ảnh điển hình của ung thư vỏ thượng thận bao gồm [5,10]:
- Khối u lớn, hình dạng không đều
- Hầu hết các khối u có kích thước lớn hơn 6 cm tại thời điểm chẩn đoán.
- Các vùng hoại tử, xuất huyết và vôi hóa, có thể dạng chấm, đốm hoặc dạng nốt không đều.
- Xâm lấn các cơ quan lân cận và hạch bạch huyết vùng.
- Xâm lấn tĩnh mạch chủ dưới (IVC) hoặc tĩnh mạch thận (9-19%).
Những bẫy hình ảnh:
- Rất hiếm khi ACC có thể có các vùng mỡ đại thể nhỏ.
- Rất ít gặp trường hợp ACC có tỷ lệ thải trừ thuốc tuyệt đối hoặc tương đối trên CT trong ngưỡng của u tuyến [10].
Hơn một nửa số bệnh nhân ACC có bệnh giai đoạn III hoặc IV tại thời điểm chẩn đoán, điều này lý giải tiên lượng xấu của bệnh, với tỷ lệ sống còn 5 năm là 50% cho giai đoạn III và 15% cho giai đoạn IV.
Do đó, điều quan trọng là phải tìm kiếm xâm lấn cơ quan lân cận, di căn hạch bạch huyết và di căn xa, thường gặp nhất ở phổi, gan hoặc xương.
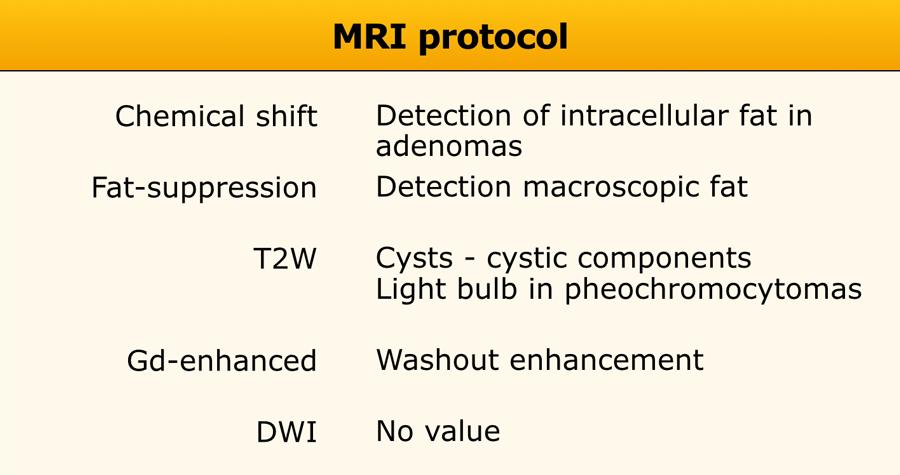
Giao thức chụp MRI
MRI thường được sử dụng như một công cụ giải quyết vấn đề sau khi CT không cho kết quả rõ ràng hoặc khi CT có thuốc cản quang bị chống chỉ định.
Giao thức chụp MRI nên bao gồm [4,5]:
- Chụp ảnh dịch chuyển hóa học với chuỗi xung đồng pha và ngược pha để phát hiện mỡ nội bào vi thể.
- Xóa mỡ để phát hiện mỡ đại thể.
- Chuỗi xung T2W để chẩn đoán nang hoặc thành phần dạng nang, đồng thời có thể hỗ trợ chẩn đoán u tủy thượng thận (pheochromocytoma) khi có dấu hiệu ‘bóng đèn’ điển hình.
- MRI động có tiêm thuốc tương phản từ gadolinium hữu ích trong việc phân biệt u tuyến (adenoma) với các tổn thương không phải u tuyến. U tủy thượng thận có thể được nhận diện nhờ đặc điểm ngấm thuốc mạnh.
Khuếch tán (DWI) không có giá trị bổ sung do sự chồng lấp đáng kể trong các giá trị ADC giữa các tổn thương tuyến thượng thận lành tính và ác tính [11].
Hầu hết các bác sĩ chẩn đoán hình ảnh sử dụng đánh giá trực quan để xác định xem có sự sụt giảm tín hiệu trên ảnh ngược pha hay không.
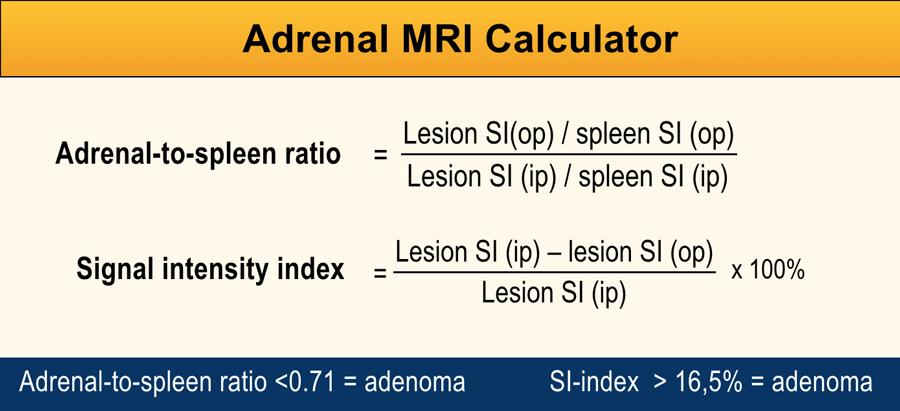
Tuy nhiên, cũng có thể đo sự thay đổi cường độ tín hiệu trong một vùng quan tâm (ROI) đặt trên tổn thương tuyến thượng thận ở ảnh ngược pha và so sánh với ảnh đồng pha, sử dụng lách làm cơ quan tham chiếu nội tại.
Tỷ số tuyến thượng thận-lách (ASR) hoặc chỉ số cường độ tín hiệu tuyến thượng thận (SI-index) có thể được tính toán bằng cách sử dụng máy tính MRI tuyến thượng thận [12,13].
ASR <0,71 và SI-index >16,5% gợi ý u tuyến thượng thận (adenoma).
Độ nhạy được báo cáo của ASR là 58 – 99% và độ đặc hiệu là 84-86%.
Chụp ảnh dịch chuyển hóa học kém nhạy hơn CT rửa thuốc trong việc phát hiện u tuyến nghèo lipid, đặc biệt khi tỷ trọng CT không tiêm thuốc từ 20 HU trở lên [13].
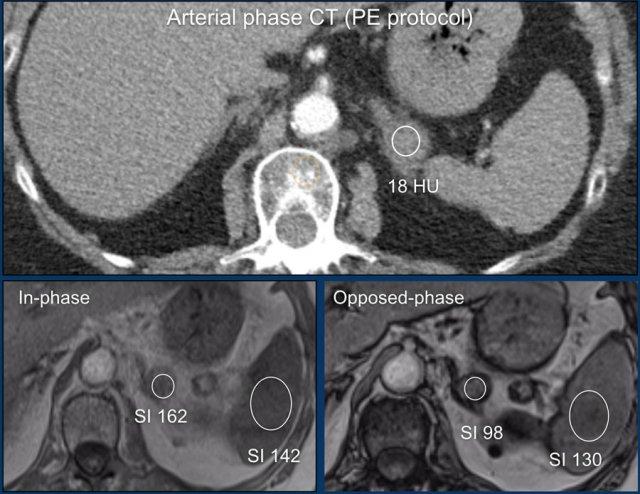
Tổn thương tuyến thượng thận này được phát hiện tình cờ trên phim chụp CT chẩn đoán thuyên tắc phổi.
Sử dụng máy tính MRI tuyến thượng thận, tỷ số tuyến thượng thận-lách (ASR) và chỉ số cường độ tín hiệu (SI-index) có thể được đo từ các vùng quan tâm (ROI) đặt bên trong tổn thương tuyến thượng thận và lách trên cả ảnh đồng pha và ngược pha.
Dựa trên cường độ tín hiệu đo được trong các ROI đặt trên tổn thương tuyến thượng thận và lách, ASR là 0,66 (< 0,71) và SII là 39,5% (> 16,5%), cho thấy đây là một u tuyến (adenoma).
PET-CT
FDG – Hình ảnh khối u tuyến thượng thận không đặc hiệu
Các khối u ác tính có chuyển hóa glucose cao hơn so với các khối u lành tính.
Đặc điểm này cho phép thực hiện chụp PET-CT với chất tương tự glucose là 18F-fluoro-deoxy-glucose (FDG).
FDG không đặc hiệu cho bất kỳ loại khối u tuyến thượng thận nào, nhưng có thể được sử dụng để phân biệt u tủy thượng thận (pheochromocytoma), u cận hạch (paraganglioma), ung thư biểu mô vỏ thượng thận và di căn tuyến thượng thận với các khối u lành tính.
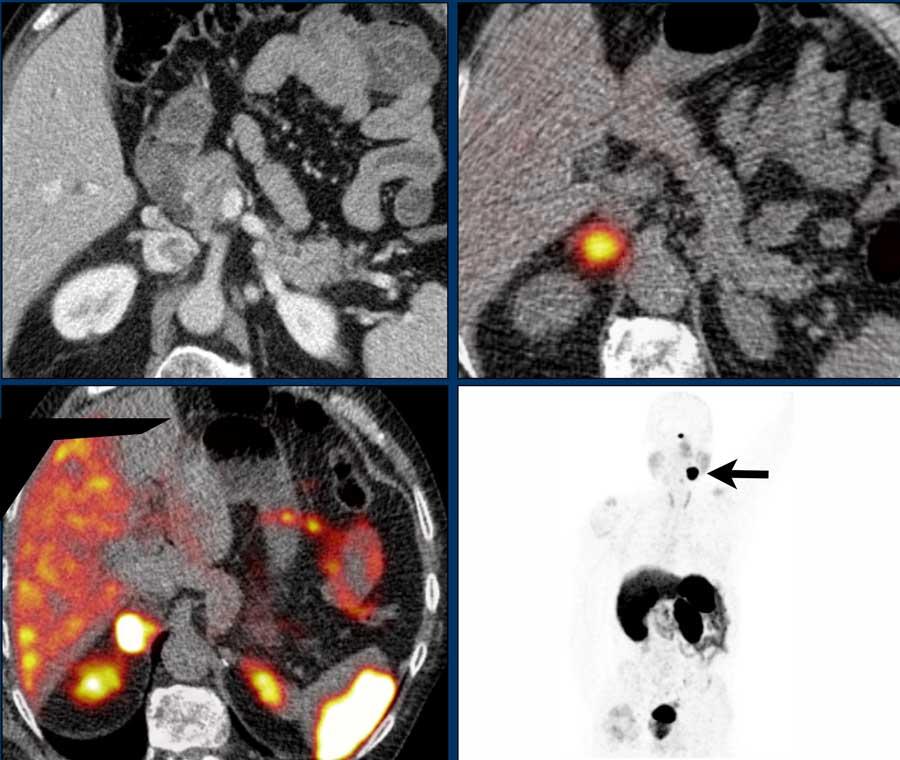
Hình ảnh thể hiện cửa sổ trung thất và cửa sổ xương của một bệnh nhân có khối u tuyến thượng thận phải kích thước lớn, ngấm thuốc không đồng nhất.
Khối u này đã được xác nhận là ung thư biểu mô vỏ thượng thận.
Có một tổn thương gan mờ nhạt, bờ không rõ ở phân thùy 6 và các thay đổi xơ cứng không đặc hiệu ở thân đốt sống T12.
Tiếp tục xem hình ảnh PET…
PET-CT thực hiện để phân giai đoạn toàn diện cho thấy sự hấp thu mạnh tại khối u tuyến thượng thận, gợi ý bản chất ác tính của khối u.
Ngoài ra còn ghi nhận sự hấp thu mạnh tại hai ổ di căn gan và một ổ di căn xương ở T12.
Khoảng 20-40% bệnh nhân ung thư biểu mô vỏ thượng thận đã có di căn tại thời điểm chẩn đoán.
PET-CT FDG toàn thân có thể phân biệt tổn thương lành tính với ác tính với độ nhạy cao (100%), nhưng độ đặc hiệu thấp hơn (87-97%).
Các trường hợp dương tính giả là do một số ít u tuyến (adenoma), u tủy thượng thận (pheochromocytoma), tổn thương viêm và nhiễm trùng có biểu hiện tương tự tổn thương ác tính [14].
Các trường hợp âm tính giả có thể gặp ở các ổ di căn xuất huyết, hoại tử hoặc kích thước nhỏ (5-10 mm), cũng như di căn từ các ung thư nguyên phát có mức độ hấp thu FDG tương đối thấp, như ung thư biểu mô tuyến xâm lấn tối thiểu hoặc khối u carcinoid [14].
Ngoài đánh giá trực quan, có thể sử dụng giá trị hấp thu chuẩn hóa (SUV) với ngưỡng cắt nhất định (SUVmax 2,68-3,7) hoặc tỷ số SUV tuyến thượng thận/gan (giá trị ngưỡng được báo cáo là 1,29-1,45) để phân biệt tổn thương tuyến thượng thận lành tính với ác tính, với độ nhạy và độ đặc hiệu cao [14, 15].
Kết hợp PET-CT FDG và CT đánh giá độ thải thuốc tuyến thượng thận (adrenal washout CT) có thể cải thiện thêm độ chính xác trong chẩn đoán ác tính tuyến thượng thận [16].
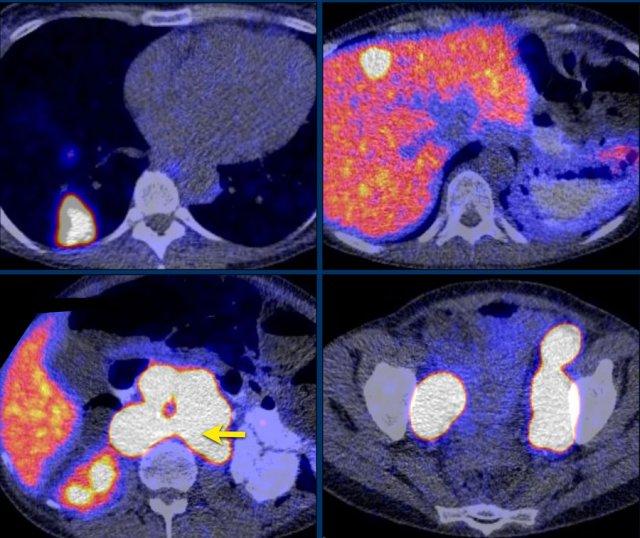
CT thì tĩnh mạch mặt cắt ngang này cho thấy một khối tuyến thượng thận phải kích thước rất lớn, nghi ngờ ác tính dựa trên kích thước lớn và tính không đồng nhất.
Tổn thương này là ung thư biểu mô vỏ thượng thận, nhưng trái với ví dụ trước, PET-CT FDG thực hiện tiếp theo cho mục đích phân giai đoạn chỉ cho thấy sự hấp thu nhẹ và chỉ ở phần ngấm thuốc mạnh nhất của khối u.
Hầu hết các ung thư biểu mô vỏ thượng thận đều có sự hấp thu FDG mạnh.
Sự thiếu hụt hấp thu FDG này có thể do khối u độ thấp với tốc độ phân bào thấp hơn hoặc có các thành phần xuất huyết hay hoại tử lớn.
CT thì tĩnh mạch mặt cắt ngang đầu tiên sau phẫu thuật, thực hiện 3 tháng sau khi cắt tuyến thượng thận trái vì ung thư biểu mô vỏ thượng thận kích thước lớn, cho thấy một nốt ngấm thuốc ở phía sau thận trái.
PET-CT FDG tái phân giai đoạn cho thấy sự hấp thu mạnh chỉ tại tổn thương này, được xác nhận là ổ di căn trên hình ảnh theo dõi tiếp theo.
Khối máu tụ dưới bao thận trái là không liên quan.
Hình ảnh đặc hiệu cho u tủy thượng thận (Pheochromocytoma)
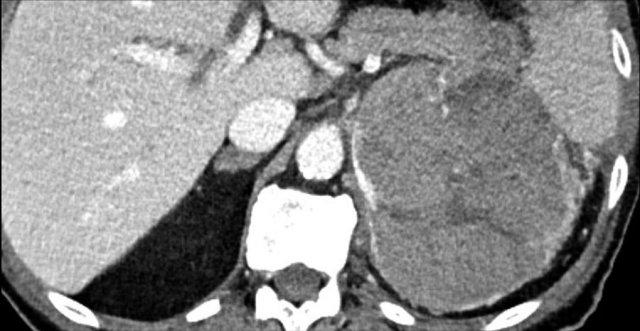
CT thì động mạch và thì tĩnh mạch mặt cắt ngang cho thấy một u tình cờ tuyến thượng thận trái tăng sinh mạch máu.
Metanephrine tự do trong huyết tương tăng cao, có giá trị chẩn đoán u tủy thượng thận (pheochromocytoma).
Phân giai đoạn tiếp theo bao gồm SPECT MIBG và PET-CT FDG, cả hai đều cho thấy sự hấp thu mạnh tại khối u tuyến thượng thận trái, nhưng không có bằng chứng bệnh di căn.
U tủy thượng thận (pheochromocytoma) và u cận hạch (paraganglioma) có nguồn gốc từ các tế bào ưa crôm (chromaffin) ở tủy thượng thận.
Đây là các tế bào thần kinh nội tiết biểu hiện thụ thể vận chuyển norepinephrine trên màng tế bào và bài tiết catecholamine, noradrenaline, dopamine cùng một số hormone khác.
Đây là cơ sở cho việc sử dụng các chất đánh dấu như 131I- và 123I-MIBG, tích lũy trong mô adrenergic, giúp xạ hình MIBG trở nên đặc hiệu cho u tủy thượng thận và u cận hạch.
18F-dihydroxyphenylalanine (DOPA) và 18F-fluorodopamine (DA) là các hợp chất đặc hiệu cho u tủy thượng thận được đánh dấu bằng 18F, có thể sử dụng cho chụp PET-CT [19].
U tủy thượng thận và u cận hạch cũng có thụ thể somatostatin và do đó có thể được hiển thị bằng các chất tương tự somatostatin.
Xạ hình somatostatin (hay Octreoscan) hiện đang dần được thay thế bởi PET-CT sử dụng các chất tương tự somatostatin gắn nhãn 68 gallium như DOTA-TOC, DOTA-NOC hoặc DOTA-TATE [19].
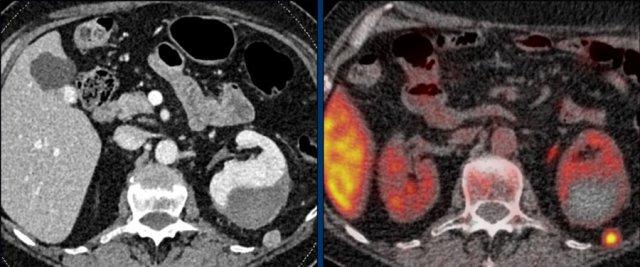
CT thì tĩnh mạch mặt cắt ngang bên trái cho thấy một tổn thương tuyến thượng thận phải kích thước lớn, ngấm thuốc không đồng nhất kèm một nang nhỏ, không thể chẩn đoán là u tuyến (adenoma) bằng CT đánh giá độ thải thuốc, do đó được xếp vào nhóm tổn thương chưa xác định.
Metanephrine tự do trong huyết tương tăng cao và tổn thương được chẩn đoán là u tủy thượng thận (pheochromocytoma).
SPECT MIBG để phân giai đoạn cho thấy sự hấp thu mạnh chỉ ở tuyến thượng thận phải.
PET-CT cũng được thực hiện, nhưng ngược lại chỉ cho thấy sự hấp thu cao hơn gan bình thường một chút.
Đây là điều rất bất thường đối với u tủy thượng thận, vốn thường có sự hấp thu FDG rất mạnh, ngay cả khi lành tính.
Nếu khối u nguyên phát thiếu sự hấp thu FDG, độ nhạy để phát hiện di căn trên PET-CT FDG sẽ rất thấp.
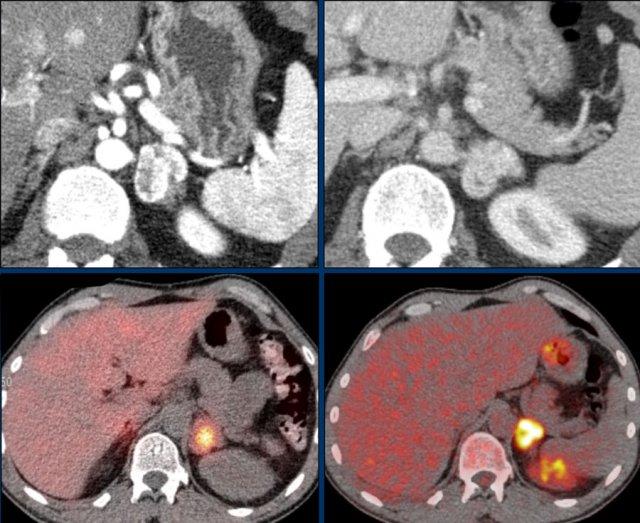
Hình ảnh phía trên bên trái là CT tầm soát thì tĩnh mạch ở bệnh nhân có đột biến gen SDHD đã biết, liên quan đến nguy cơ cao phát triển u tủy thượng thận và u cận hạch.
Có một khối u tuyến thượng thận phải tăng sinh mạch máu.
SPECT MIBG được thực hiện cho thấy sự hấp thu mạnh, giúp xác nhận chẩn đoán u tủy thượng thận.
Một năm sau, tầm soát được thực hiện bằng PET-CT 68 Ga-DOTATATE.
Hình ảnh cho thấy sự hấp thu mạnh ở tuyến thượng thận phải, đồng thời cũng ghi nhận sự hấp thu mạnh tại một khối u cầu cảnh (glomus caroticum) bên trái như thấy trên ảnh MIP mặt phẳng đứng dọc bên phải.
Sự hấp thu DOTATATE ở lách và tuyến yên là bình thường, cũng như sự bài tiết bình thường qua thận xuống bàng quang.
U tủy thượng thận (pheochromocytoma) biểu hiện thụ thể somatostatin, khiến chúng phù hợp để hiển thị bằng chất tương tự somatostatin.
Trong trường hợp này, DOTATOC gắn nhãn 68 gallium được sử dụng.
Bệnh nhân này biểu hiện bệnh di căn lan rộng đến phổi, gan và các hạch bạch huyết sau phúc mạc sau khi phẫu thuật cắt bỏ u tủy thượng thận.
Tiếp tục xem PET-CT…
PET-CT của cùng bệnh nhân với DOTATOC gắn nhãn 68 gallium.
Đánh giá nội tiết
Có đến 15% tổng số khối u tuyến thượng thận có chức năng nội tiết:
- U tuyến tiết cortisol (rất phổ biến).
- U tủy thượng thận (pheochromocytoma) tiết catecholamine (ít gặp).
- U tuyến tiết aldosterone (ít gặp).
- Ung thư vỏ thượng thận tiết glucocorticoid hoặc androgen (cực kỳ hiếm gặp).
Hướng dẫn hiện hành của Hội Nội tiết Châu Âu (ESE), Hiệp hội Bác sĩ Nội tiết Lâm sàng Hoa Kỳ (AACE) và Trường Môn X quang Hoa Kỳ (ACR) [2,3] khuyến nghị thực hiện đánh giá sinh hóa ban đầu cho tất cả các trường hợp u tuyến thượng thận tình cờ phát hiện, nhằm loại trừ u tủy thượng thận (pheochromocytoma), hội chứng Cushing dưới lâm sàng và cường aldosterone.
Các hormone sau đây cần được đánh giá ở tất cả bệnh nhân có u tuyến thượng thận tình cờ phát hiện:
- Nghiệm pháp ức chế dexamethasone qua đêm để loại trừ tình trạng dư thừa cortisol.
- Metanephrine tự do trong huyết tương hoặc metanephrine phân đoạn trong nước tiểu để chẩn đoán hoặc loại trừ u tủy thượng thận (pheochromocytoma).
Các hormone sau đây cần được đánh giá có điều kiện:
- Tỷ lệ aldosterone/renin để loại trừ cường aldosterone nguyên phát ở bệnh nhân có triệu chứng tăng huyết áp hoặc hạ kali máu không rõ nguyên nhân.
- Hormone sinh dục và các tiền chất steroid ở bệnh nhân nghi ngờ ung thư vỏ thượng thận (ACC).